文献分享:肿瘤免疫逃逸机制及应对策略
本文对Li等发表于《Journal of Biomedical Science》的综述文章《Immune evasion in cell‑based immunotherapy: unraveling challenges and novel strategies》进行系统分析。该文献聚焦细胞免疫治疗(Cell-based Immunotherapies, CBIs)中肿瘤免疫逃逸这一核心难题,系统整合了近年来肿瘤免疫逃逸与CBIs相关的基础研究及临床数据,形成了“逃逸机制-应对策略-生物标志物”的完整研究体系,为CBIs的优化提供了重要支撑。
一、研究背景概述
细胞免疫治疗是肿瘤治疗领域的革命性突破,其核心原理是体外改造、回输活化免疫细胞,利用机体自身免疫系统精准杀伤肿瘤细胞,代表了个体化精准肿瘤治疗的全新方向。以 CAR‑T、CAR‑NK 为代表的细胞免疫治疗,通过基因工程赋予免疫细胞特异性识别肿瘤抗原的能力,并强化其细胞毒性效应,在既往难治性恶性肿瘤中展现出前所未有的疗效,显著突破了传统放化疗、靶向治疗的局限。
尽管 CBIs 在血液肿瘤中取得里程碑式成功,但临床应用仍存在诸多瓶颈:脱靶效应、实体瘤疗效有限、肿瘤免疫抑制微环境、细胞制备工艺不稳定等问题,严重制约其广泛应用。其中,肿瘤免疫逃逸是导致 CBIs 治疗失败、疾病复发的最关键因素。肿瘤可通过多种策略逃避改造后免疫细胞的攻击:一是下调或丢失治疗靶点抗原,降低被免疫细胞识别的概率;二是高表达 PD‑L1 等免疫检查点分子,直接抑制免疫细胞活化;三是构建高度免疫抑制的肿瘤微环境(TME),招募抑制性免疫细胞、分泌免疫抑制因子,系统性削弱免疫应答;四是诱导免疫细胞耗竭与功能异常,使 CBIs 难以发挥持久抗肿瘤作用。
因此,系统解析肿瘤针对 CBIs 的免疫逃逸机制,明确 TME 调控、抗原表达缺失、抑制信号激活等关键环节,并探索可逆转免疫逃逸的联合治疗、检查点阻断、基因编辑等优化策略,对提升 CBIs 疗效、延长患者生存、推动细胞免疫治疗临床转化具有至关重要的科学意义与临床价值。
二、肿瘤免疫逃逸的主要机制
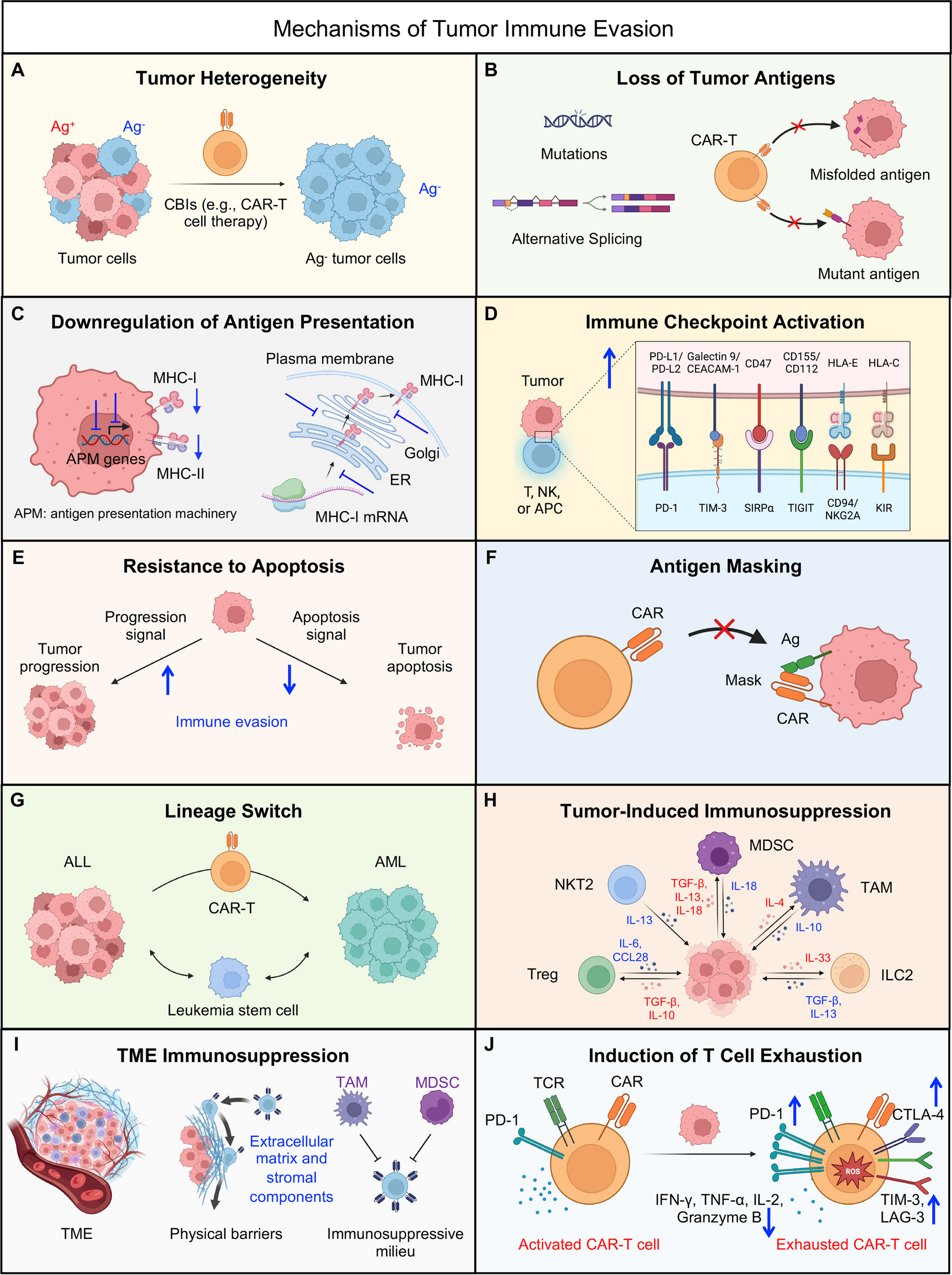
在文献中,作者将肿瘤免疫逃逸机制系统归纳为十大类,涵盖肿瘤细胞自身特性改变、TME调控及免疫细胞功能异常三个核心层面,各类机制相互协同、相互关联,形成了复杂的免疫逃逸网络。
(一)肿瘤细胞自身特性改变相关逃逸机制
1、肿瘤异质性
同一肿瘤内细胞表型、基因差异大,部分癌细胞天生缺少治疗靶点(如 CD19 阴性亚群),CAR-T 治疗后这类细胞会快速增殖导致复发,让单一靶点治疗难以彻底清除肿瘤。
2、肿瘤抗原丢失
这是最常见的逃逸方式。癌细胞通过基因突变、异常剪接,让 CD19、BCMA 等靶抗原缺失、功能异常或无法表达在细胞表面,直接躲避免疫细胞识别。
3、抗原提呈下调
癌细胞通过降低 MHC 分子表达、干扰抗原加工转运、减少共刺激分子,让抗原无法正常呈递给免疫细胞,即使有靶点也难以被识别激活。
4、抵抗凋亡能力增强
癌细胞高表达 Bcl-2、Bcl-xL 等抗凋亡蛋白,抑制免疫细胞诱导的凋亡反应,即使被攻击也能存活增殖。
5、抗原遮蔽
癌细胞表面被 CAR 结构、唾液黏蛋白等物质包裹,遮挡靶抗原,让免疫细胞无法结合识别,引发治疗失败。
6、谱系转换
多见于 MLL 重排型白血病,癌细胞在免疫压力下发生表型转变,丢失原有靶点,转为其他细胞类型,使 CAR-T 完全失效。
(二)肿瘤微环境(TME)调控相关逃逸机制
1、免疫抑制细胞浸润
肿瘤招募 TAMs、MDSCs、Tregs 等抑制性细胞,分泌抑制因子、表达 PD-L1,直接压制免疫细胞的活化与杀伤功能。
2、免疫抑制分子分泌
肿瘤大量释放 TGF-β、IL-10、腺苷等物质,全面抑制免疫细胞功能,同时促进肿瘤侵袭,形成免疫抑制环境。
3、细胞外基质(ECM)屏障
肿瘤过度分泌胶原、蛋白聚糖,形成致密物理屏障,阻挡免疫细胞进入肿瘤内部发挥作用。
4、异常血管形成
肿瘤血管结构紊乱、通透性差,阻碍免疫细胞浸润,同时引发缺氧,进一步上调 PD-L1 等抑制分子,形成恶性循环。
(三)免疫细胞功能异常相关逃逸机制
1、免疫检查点激活
肿瘤高表达 PD-L1、CTLA-4、TIM-3 等检查点分子,与免疫细胞结合后传递抑制信号,直接关停免疫细胞的杀伤能力。
2、T 细胞耗竭
长期肿瘤刺激 + 抑制微环境,使 T 细胞功能下降、细胞因子分泌减少、抑制受体持续高表达,失去抗肿瘤能力,部分可通过检查点阻断恢复。
三、应对肿瘤免疫逃逸的多种策略
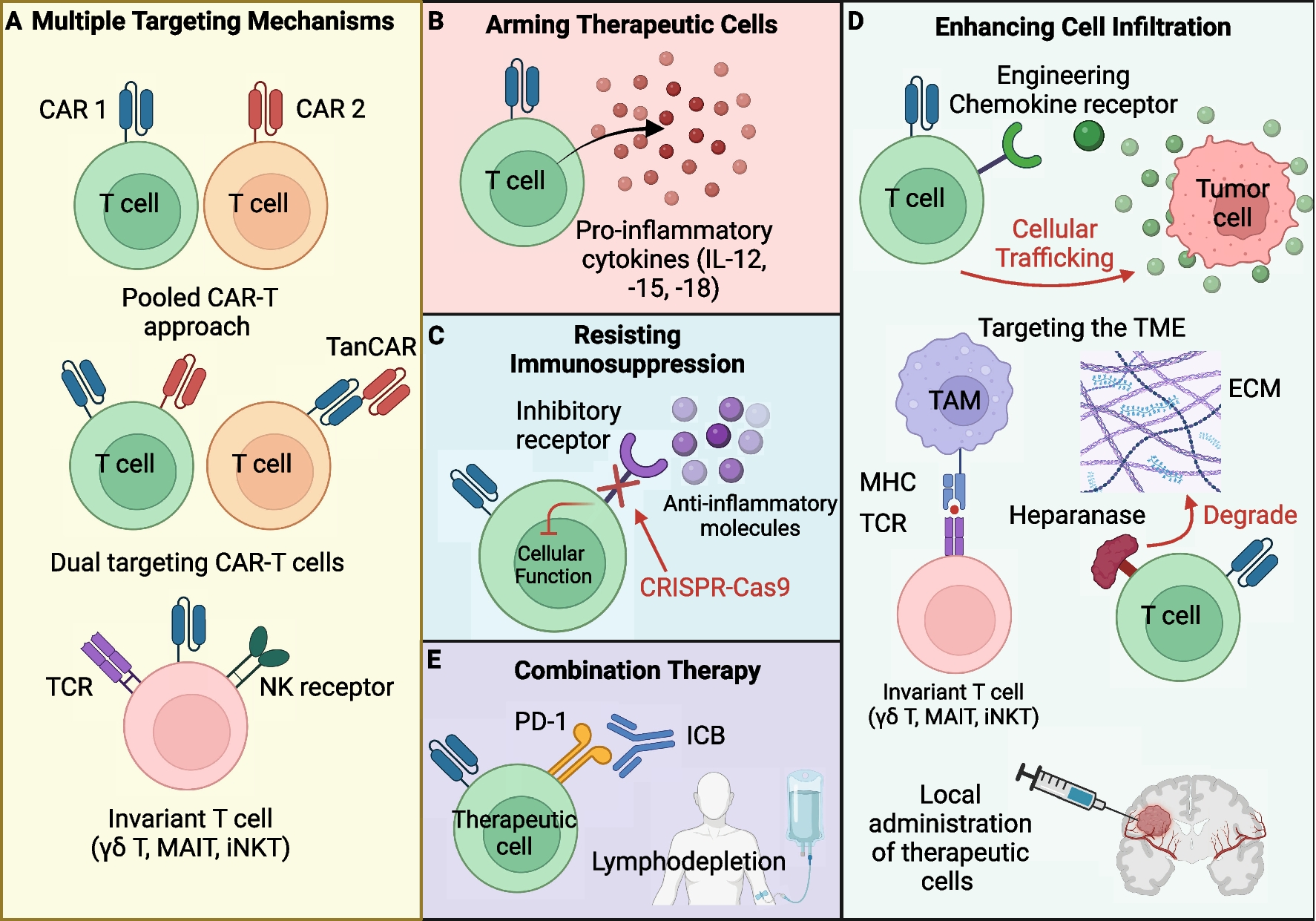
针对上述肿瘤免疫逃逸的核心机制,文章中提出了五大类针对性的工程化策略,重点聚焦于增强CBIs的肿瘤识别能力、存活能力、TME浸润能力及功能维持能力,通过多维度、系统性的改造,打破肿瘤免疫逃逸网络,提升CBIs的治疗效果。
(一)多靶点工程改造:破解抗原逃逸与肿瘤异质性
核心思路是同时识别多个肿瘤抗原,降低逃逸概率。
1、多靶点 CAR 改造:采用混合 CAR-T、双靶点 CAR、串联 CAR(TanCAR)技术,让免疫细胞同时识别两个靶点,临床缓解率可达 70%–86%,大幅减少因抗原丢失导致的复发。
2、使用非常规免疫细胞:NK、iNKT、γδT 等细胞可通过自身受体识别肿瘤,不依赖 MHC 抗原呈递,能有效对抗抗原下调或丢失,适合 CAR 改造。
(二)增强治疗细胞持久性:对抗 T 细胞耗竭与免疫抑制
通过改造延长免疫细胞在体内的存活与活性。
1、细胞因子武装:让 CAR-T 分泌 IL-15、IL-18 等,增强增殖、减少凋亡、降低 PD-1 表达;目前多用诱导型分泌,避免细胞因子风暴毒性。
2、记忆表型诱导:将 CAR-T 诱导为干细胞样 / 中心记忆表型(高表达 CD27、CD45RO),提升持久性与长期抗肿瘤能力。
(三)抵抗 TME 免疫抑制:打破抑制信号网络
直接让治疗细胞对抑制信号 “免疫”,并清除抑制细胞。
1、阻断抑制通路:用 CRISPR 敲除 TGF-β 受体、腺苷 A2A 受体,或表达显性负性受体,使 CAR-T 不受 TGF-β、腺苷等抑制分子影响。
2、清除抑制细胞:改造免疫细胞靶向并清除 TAMs、MDSCs 等免疫抑制细胞,重塑肿瘤微环境。
(四)增强浸润能力:突破肿瘤物理屏障
解决免疫细胞进不去肿瘤内部的问题。
1、趋化受体改造:过表达 CXCR2、CCR6、CCR2b 等受体,引导 CAR-T 精准向肿瘤迁移聚集。
2、基质降解:让 CAR-T 表达乙酰肝素酶(HPSE),降解细胞外基质,打通进入肿瘤的通道。
3、局部递送:直接将 CAR-T 注射到肿瘤区域,提高局部浓度、提升疗效。
(五)联合治疗:协同增效,全面破防
单一策略不足,多方案组合效果更佳。
1、+ 免疫检查点抑制剂:解除 PD-1/PD-L1 抑制,恢复 T 细胞功能。
2、+ 放化疗:放疗增强免疫原性、破坏屏障;化疗清除抑制细胞、利于 CAR-T 扩增。
3、+mRNA 疫苗(CARVac):激活并扩增 CAR-T,低剂量即可控制肿瘤,实体瘤客观缓解率可达 33%。
四、细胞免疫治疗相关生物标志物
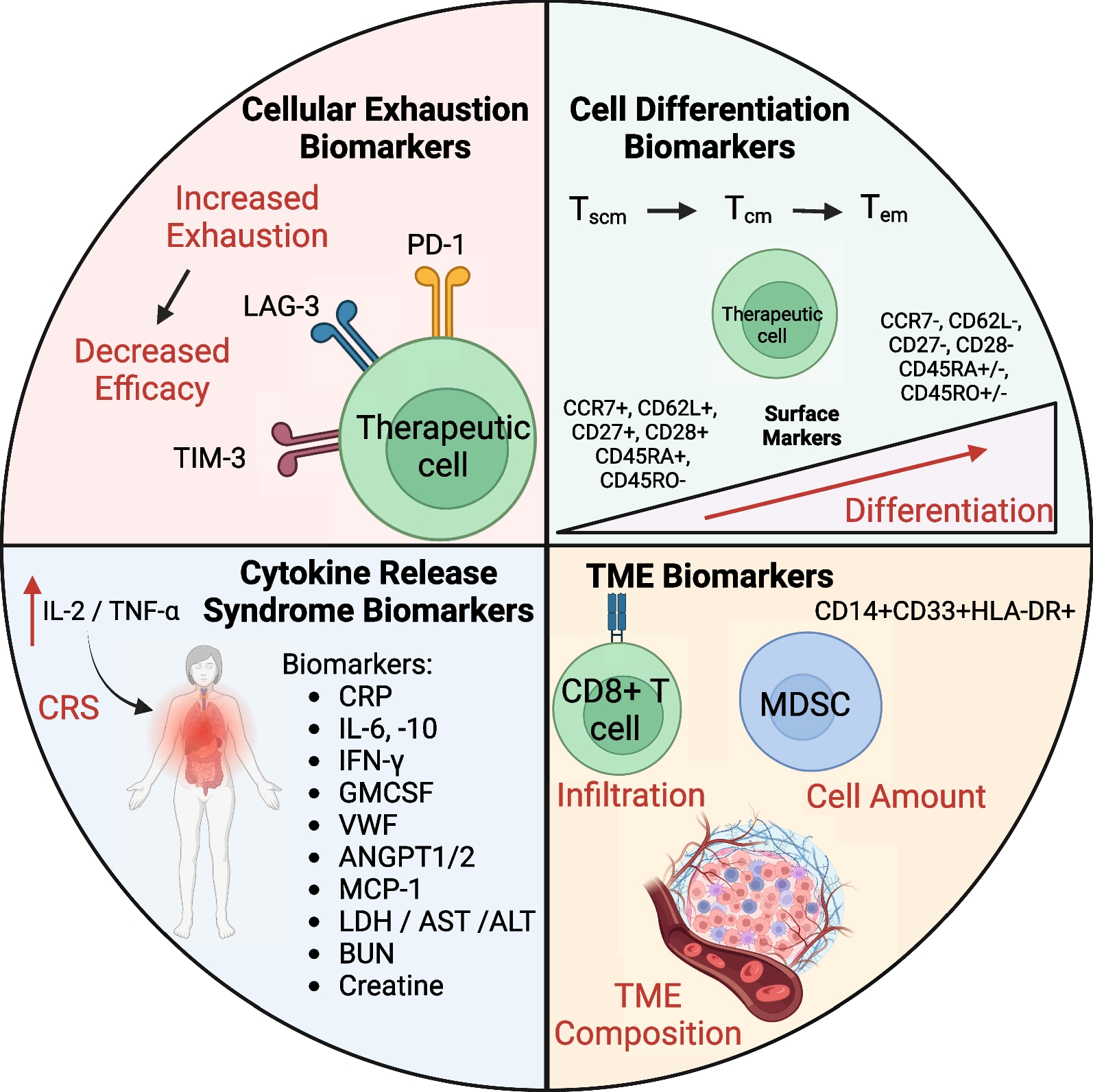
结合肿瘤免疫逃逸机制与CBIs治疗特点,文献系统梳理了四类核心生物标志物,这些标志物不仅可用于预测CBIs治疗响应、监测治疗过程中的不良反应,还能评估TME免疫状态,为临床个性化治疗方案的制定提供重要参考,是“逃逸机制-应对策略-生物标志物”研究体系的重要组成部分。
(一)免疫细胞耗竭标志物
用于判断免疫细胞是否 “耗竭”,预测治疗效果。
● 核心:PD-1、LAG-3、TIM-3 等高表达,提示 T 细胞功能下降、杀伤减弱,治疗效果差。
● 辅助:IL-2、IFN-γ 减少,IL-10 升高,提示免疫抑制加重。
● 意义:可提前预判疗效,指导是否联用免疫检查点抑制剂。
(二)免疫细胞分化标志物
用于评估 CAR-T 存活与长期疗效。
● 记忆型 T 细胞(Tscm、Tcm,高表达 CD27、CD62L、CD45RO)比例越高,CAR-T 存活越久、复发率越低。
● CD127 高表达提示细胞自我更新能力强,更能抵抗肿瘤微环境抑制。
(三)细胞因子释放综合征(CRS)标志物
用于监测 CAR-T 最常见的严重副作用。
● 关键:IL-6 是核心指标,水平越高,CRS 越重。
● 辅助:IL-10、CRP、VWF 升高提示炎症与内皮损伤,可提前预警严重反应,及时干预。
(四)肿瘤微环境(TME)标志物
评估免疫抑制强度,指导治疗方案。
● 免疫抑制细胞:MDSCs、Tregs、TAMs 比例越高,治疗越难起效。
● 抑制分子:TGF-β、IL-10、PD-L1 高表达,提示微环境恶劣,需加强 “破抑制” 策略。
● 基质指标:胶原蛋白、纤维连接蛋白高,提示屏障厚,需增强免疫细胞浸润能力。
五、总结
本篇综述文章,核心贡献在于系统总结了细胞免疫治疗中肿瘤免疫逃逸的主要机制,并针对性地提出了多种工程化应对策略,同时梳理了四类核心细胞免疫治疗相关生物标志物,通过清晰的综述图直观呈现了“逃逸机制-应对策略-生物标志物”的完整研究体系,具有重要的研究价值与学术贡献。从研究价值来看,该文献首次系统性地整合了十大类肿瘤免疫逃逸机制,明确了各类机制的分子基础和相互作用,填补了现有研究中机制分类不系统、策略与机制对应性不强的空白。其中提出的多靶点改造、细胞因子武装、TME重塑等策略,具有较强的临床转化潜力,为下一代CBIs的研发提供了明确的方向。梳理的生物标志物体系,为临床个性化治疗、疗效监测提供了重要参考,推动CBIs从“通用型”向“个性化”转变。
参考文献
Li YR, Halladay T, Yang L. Immune evasion in cell-based immunotherapy: unraveling challenges and novel strategies. J Biomed Sci. 2024 Jan 12;31(1):5. doi: 10.1186/s12929-024-00998-8. PMID: 38217016; PMCID: PMC10785504.
EnkiLife恩玑生命产品:
