Podocyte GOLM1:糖尿病肾病进展的“隐形推手”?——解析《Adv. Sci.》最新研究成果
糖尿病肾病(DN)作为糖尿病最具破坏性的并发症之一,全球患病率逐年攀升,约40%的2型糖尿病患者和30%的1型糖尿病患者会遭受肾脏损伤,最终可能进展为终末期肾病,但其发病机制尚未完全阐明,临床仍缺乏高效的靶向治疗手段。那么,是否存在一种关键分子,在糖尿病肾病的发生发展中扮演核心角色,成为潜在的治疗靶点?2025年7月,研究人员在《Advanced Science》上发表了题为《Inhibition of AMPKα Pathway by Podocyte GOLM1 Exacerbates Diabetic Nephrology in Mice》的研究论文,通过体内外多模型、多维度实验,首次揭示了足细胞中GOLM1分子在糖尿病肾病进展中的致病作用及调控机制,为临床治疗提供了全新的思路,这也正是众多肾脏疾病研究人员长期关注并渴望突破的关键方向——找到糖尿病肾病中特异性调控足细胞损伤的核心分子,打破现有治疗瓶颈。
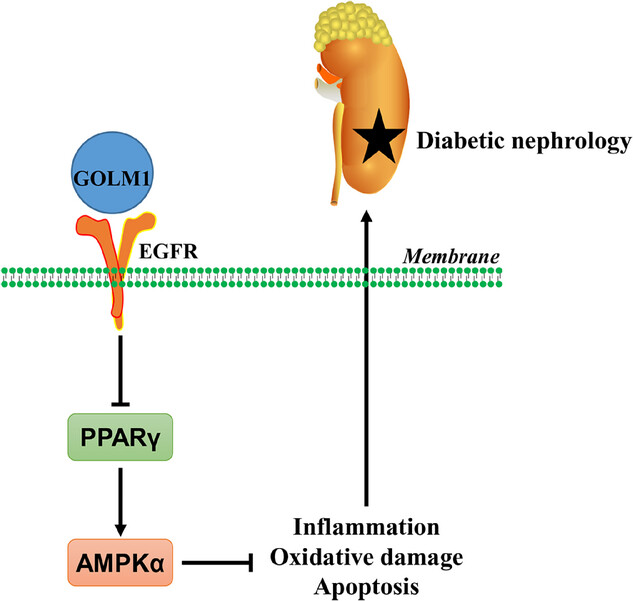
一、研究背景与方法
糖尿病肾病的核心病理特征包括肾脏炎症、氧化损伤、足细胞凋亡及肾纤维化,其中足细胞损伤被认为是糖尿病肾病发生的始动因素之一,其数量减少和功能异常往往早于临床可检测的蛋白尿出现,但目前调控足细胞损伤的关键分子及机制仍不明确。GOLM1作为一种已知的癌基因,在多种恶性肿瘤中高表达并促进肿瘤进展,近年来有研究发现其与炎症、氧化应激相关,但在糖尿病肾病中的作用及调控机制尚未有报道。基于此,该研究团队整合5个GEO数据集,筛选出糖尿病肾病小鼠模型中15个重叠的差异表达基因(DEGs),最终锁定GOLM1作为研究对象,旨在明确其在糖尿病肾病中的表达特征、功能及分子机制。研究方法上,该研究采用体内外结合的方式,体内构建1型糖尿病(STZ注射)和2型糖尿病(HFD喂养)小鼠模型,同时建立足细胞特异性GOLM1敲除(Golm1pKO)和过表达(Golm1pTG)小鼠模型,通过检测血清肾功能指标、肾脏病理染色、炎症及氧化应激相关标志物等,明确GOLM1对糖尿病肾病的影响;体外分离原代足细胞,采用高糖(HG)刺激模拟糖尿病环境,通过细胞活力检测、ROS检测、Western Blot、免疫沉淀(IP)、实时荧光定量PCR(qRT-PCR)等技术,探究GOLM1的作用机制;同时纳入糖尿病肾病患者和健康对照者的肾活检样本及血清样本,验证GOLM1的临床相关性,所有数据采用SPSS软件进行统计分析,以P<0.05为差异有统计学意义。
二、结果分析:解锁GOLM1调控糖尿病肾病的关键密码
1、GOLM1在糖尿病肾病中异常升高,且与肾功能损伤密切相关
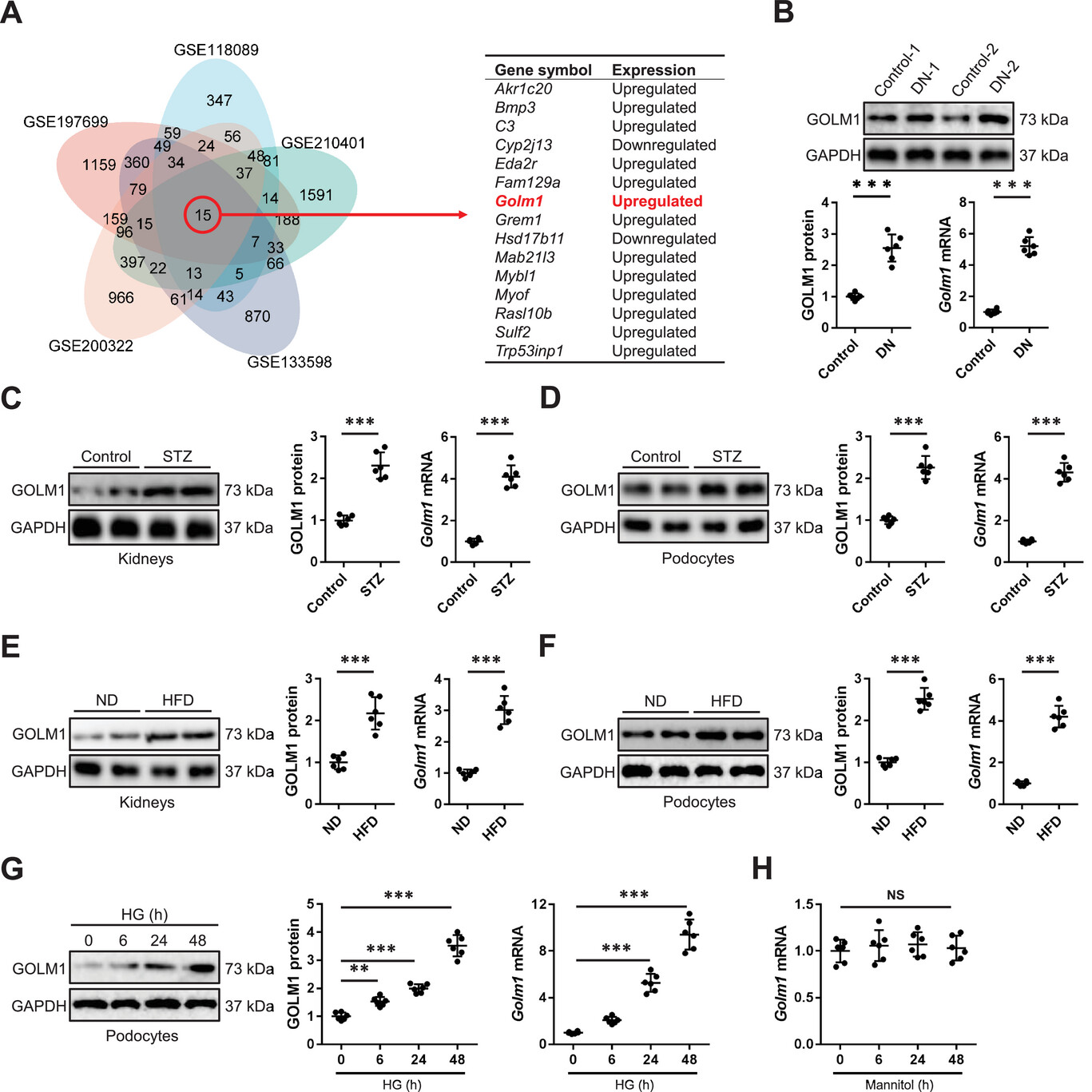
研究的第一步,团队便通过多维度实验,勾勒出GOLM1在糖尿病肾病中的“异常轨迹”。在临床样本中,糖尿病肾病患者肾脏组织中GOLM1的mRNA和蛋白水平均显著高于健康对照者,这一现象在两种糖尿病小鼠模型中得到了完美复刻——STZ诱导的1型糖尿病小鼠和HFD诱导的2型糖尿病小鼠,其肾脏组织及分离的原代足细胞中,GOLM1的表达均明显上调。更关键的是,这种上调并非肾脏所有细胞的普遍现象,体外实验证实,高糖刺激仅能显著增加足细胞中GOLM1的表达,而对肾脏内皮细胞、系膜细胞等其他细胞无明显影响,暗示GOLM1的作用具有足细胞特异性。
作为一种被定义为新型糖异生激素的分子,GOLM1的血清水平是否能成为糖尿病肾病的潜在生物标志物?进一步的临床和动物实验给出了肯定答案:糖尿病肾病患者的血清GOLM1水平显著升高,且与慢性肾病(CKD)分期正相关,血清GOLM1浓度越高,患者的血清肌酐(Cr)水平越高、估算肾小球滤过率(eGFR)越低,提示其与肾功能损伤程度密切相关。在糖尿病小鼠模型中,血清GOLM1水平同样显著升高,且体外高糖刺激能促进足细胞向培养基中分泌GOLM1,这一发现不仅证实了GOLM1在糖尿病肾病中的异常表达,更提示其可能通过自分泌方式发挥作用,为后续机制研究埋下伏笔。这些结果清晰地表明,GOLM1的异常升高是糖尿病肾病进展中的一个关键特征,其表达水平与疾病严重程度紧密相连,有望成为糖尿病肾病诊断和病情评估的潜在生物标志物。
2、足细胞GOLM1的“得”与“失”,直接决定糖尿病肾病的走向
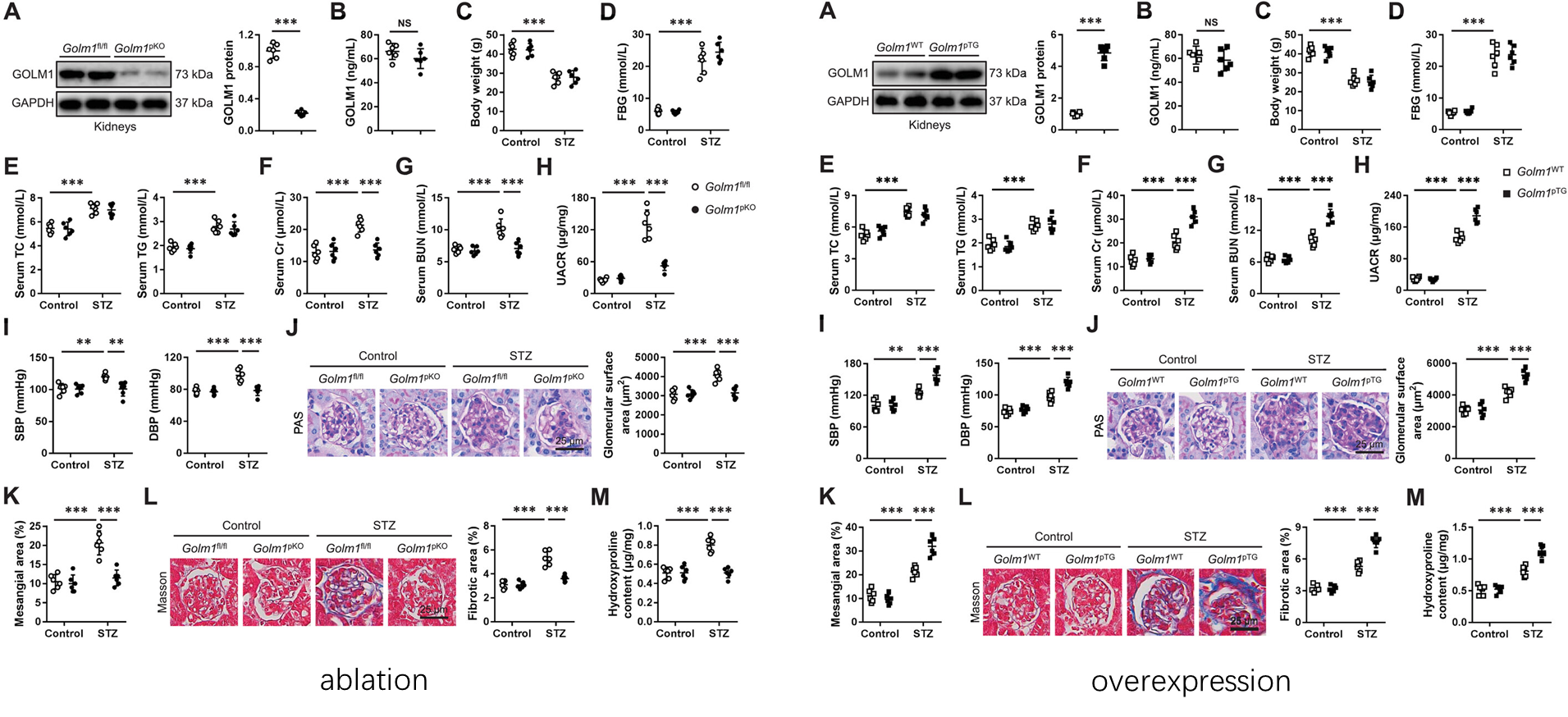
为明确足细胞中GOLM1的具体功能,研究团队构建了足细胞特异性GOLM1敲除和过表达小鼠模型,通过失去和获得GOLM1功能,观察其对糖尿病肾病的影响,这也是整个研究的核心突破点。在STZ诱导的1型糖尿病模型中,足细胞特异性敲除GOLM1后,小鼠的血清Cr、尿素氮(BUN)和尿白蛋白/肌酐比值(UACR)显著降低,糖尿病诱导的高血压也得到明显缓解,肾脏病理检查显示,肾小球肥大、系膜区扩张和肾纤维化程度均显著减轻,意味着足细胞中GOLM1的缺失能有效延缓糖尿病肾病的进展。
与之相反,足细胞特异性过表达GOLM1则会产生负面效果。过表达小鼠在STZ或HFD诱导下,肾功能损伤进一步加重,血清肾功能指标显著升高,肾脏病理损伤更为严重,肾小球肥大和肾纤维化程度明显加剧。更重要的是,无论是敲除还是过表达GOLM1,均不影响小鼠的体重、空腹血糖(FBG)、总胆固醇(TC)、甘油三酯(TG)等全身代谢指标,表明GOLM1对糖尿病肾病的调控作用是特异性作用于肾脏,而非通过影响全身代谢实现。这一系列实验构建了一个清晰的逻辑链:足细胞中GOLM1的异常高表达是糖尿病肾病进展的重要驱动因素,抑制其表达可延缓疾病进展,而其过度表达则会加速疾病恶化,为后续靶向GOLM1的治疗提供了直接的功能证据。
3、GOLM1通过加剧炎症和氧化损伤,推动足细胞凋亡与肾损伤
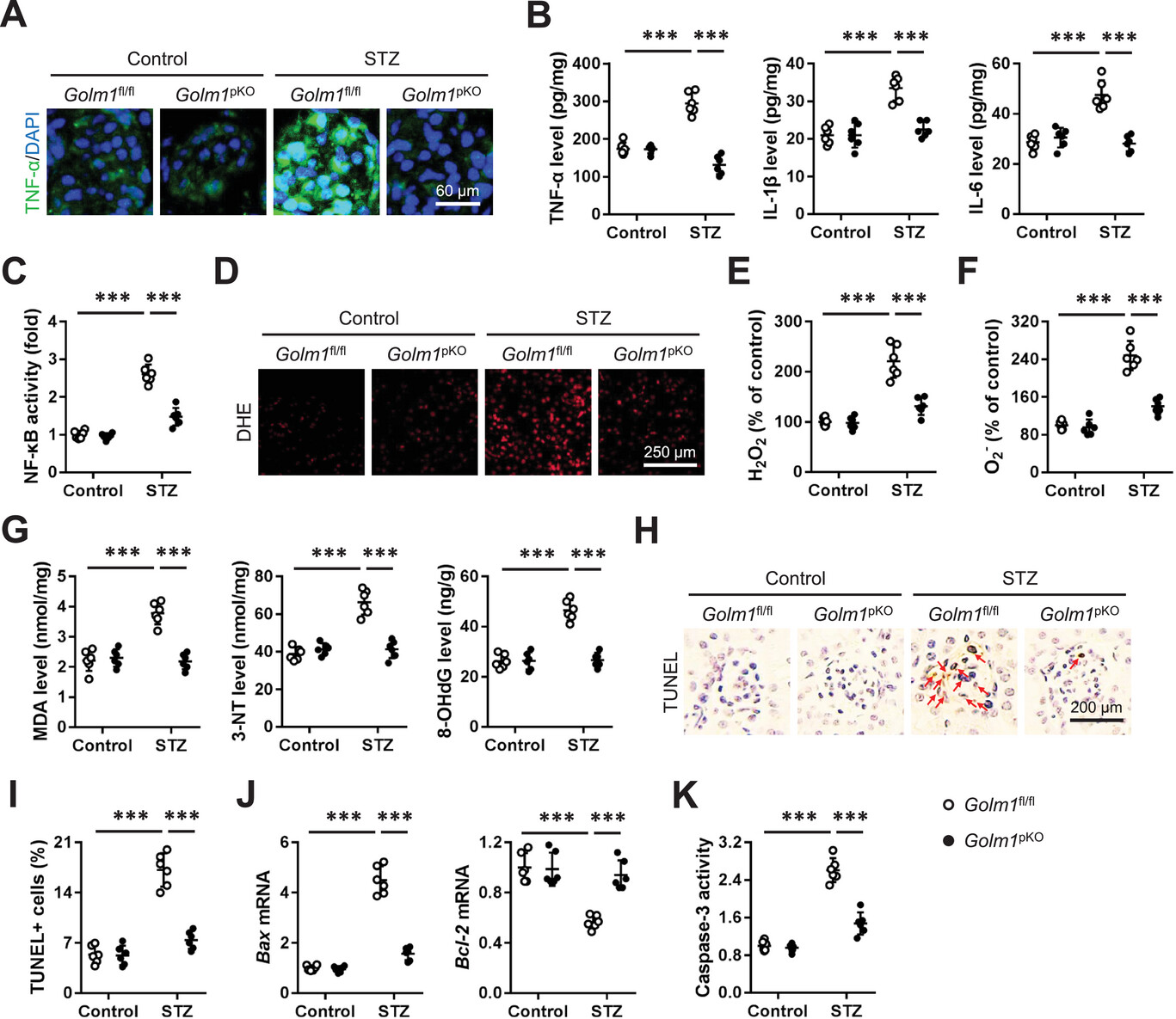
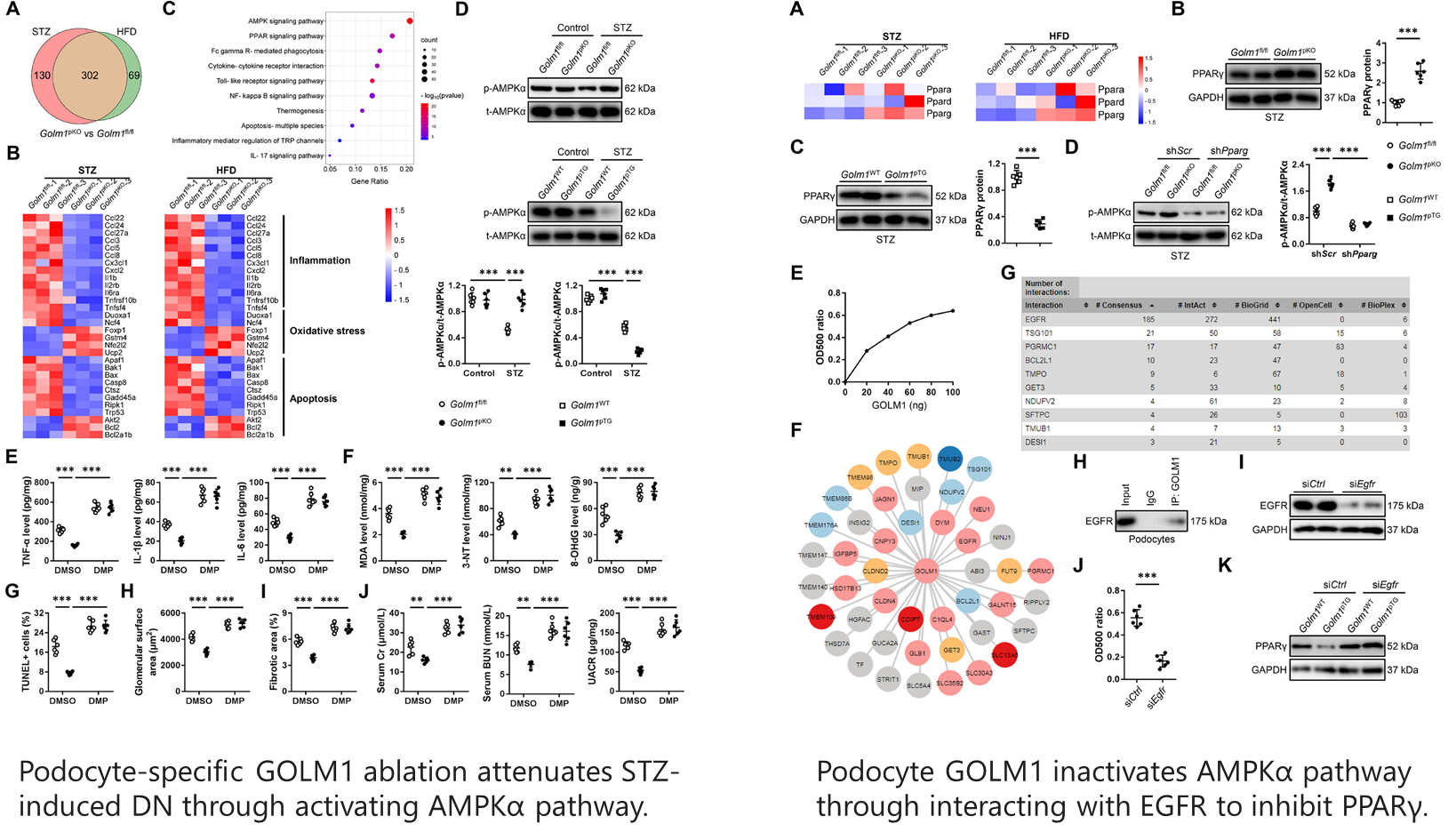
明确了GOLM1的功能后,研究团队进一步探究其调控糖尿病肾病的具体途径。炎症和氧化损伤是糖尿病肾病的两大核心病理机制,二者协同作用,促进足细胞凋亡和肾纤维化。实验发现,在STZ诱导的糖尿病小鼠中,足细胞特异性敲除GOLM1后,肾脏组织中肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)等促炎因子的水平显著降低,核因子-κB(NF-κB)的转录活性也受到明显抑制,而NF-κB作为炎症反应的核心转录因子,其激活正是糖尿病肾病中炎症加剧的关键。
在氧化损伤方面,敲除GOLM1能显著减少糖尿病小鼠肾脏中活性氧(ROS)的产生,降低丙二醛(MDA)、3-硝基酪氨酸(3-NT)、8-羟基脱氧鸟苷(8-OHdG)等氧化损伤标志物的水平,这些标志物的降低意味着肾脏细胞的氧化损伤得到有效缓解。与此同时,足细胞凋亡也明显减少,表现为TUNEL阳性细胞数量减少、促凋亡基因Bax表达降低、抗凋亡基因Bcl-2表达升高、胱天蛋白酶-3(Caspase-3)活性降低。反之,足细胞过表达GOLM1则会显著加剧炎症反应、氧化损伤和足细胞凋亡。这一结果揭示了GOLM1调控糖尿病肾病的重要机制:通过促进炎症反应和氧化损伤,加速足细胞凋亡,进而推动肾脏功能损伤和纤维化进展,为后续机制的深入探究指明了方向。
4、GOLM1通过EGFR/PPARγ/AMPKα通路,调控糖尿病肾病进展
为彻底解锁GOLM1调控糖尿病肾病的分子密码,研究团队通过RNA测序分析,筛选出GOLM1敲除小鼠与野生型小鼠肾脏中的差异表达基因,发现这些基因主要富集在AMPK信号通路,而AMPKα作为AMPK通路的核心分子,其磷酸化水平在糖尿病小鼠肾脏中显著降低,而足细胞特异性敲除GOLM1能恢复其磷酸化水平,过表达GOLM1则会进一步抑制其磷酸化。为验证AMPKα的作用,研究人员使用AMPKα特异性抑制剂DMP处理小鼠和足细胞,结果发现,DMP能完全消除GOLM1敲除带来的抗炎、抗氧化、抗凋亡及肾脏保护作用,证实AMPKα通路是GOLM1调控糖尿病肾病的关键下游通路。
进一步研究发现,PPARγ作为AMPKα通路的上游调控因子,其表达在GOLM1敲除小鼠肾脏中显著升高,过表达GOLM1则显著降低其表达,且沉默PPARγ能有效阻断GOLM1敲除对AMPKα的激活作用及肾脏保护效应,表明GOLM1通过抑制PPARγ,进而 inactivation AMPKα通路。那么,GOLM1又是如何抑制PPARγ的?通过蛋白质相互作用分析和免疫沉淀实验,研究团队发现,GOLM1能与足细胞膜上的表皮生长因子受体(EGFR)相互作用,而EGFR的敲除能阻断GOLM1对PPARγ的抑制作用,恢复PPARγ的表达。结合此前发现的“高糖能促进足细胞分泌GOLM1”的结论,一个完整的分子机制得以清晰呈现:高糖刺激下,足细胞分泌的GOLM1通过自分泌方式与自身细胞膜上的EGFR结合,抑制PPARγ的表达,进而 inactivation AMPKα通路,最终加剧炎症反应、氧化损伤和足细胞凋亡,推动糖尿病肾病进展。
5、GOLM1中和抗体,为糖尿病肾病治疗提供新策略
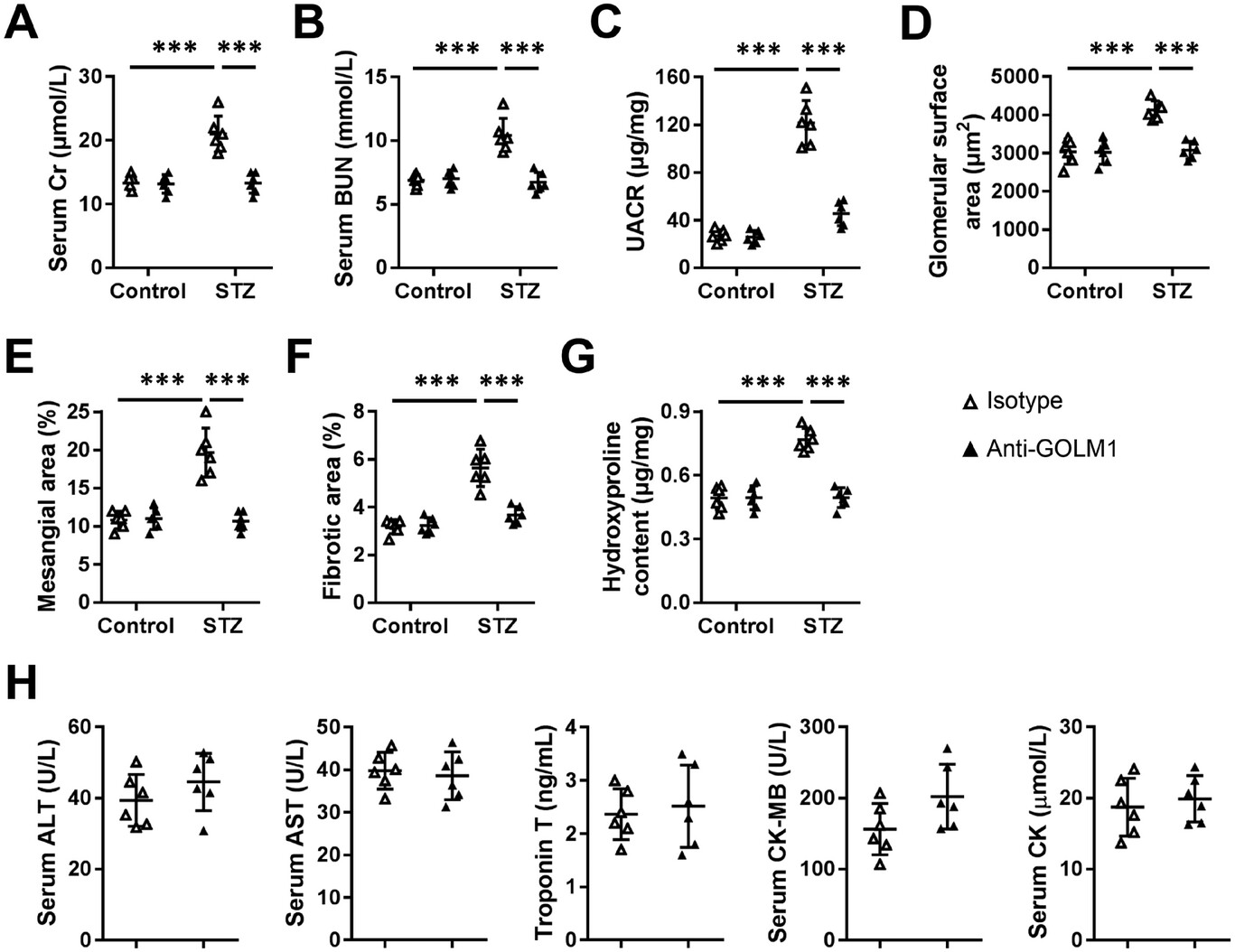
基于上述研究发现,研究团队进一步探索了靶向GOLM1的治疗潜力,选用GOLM1中和抗体处理糖尿病小鼠,结果显示,抗体治疗能显著降低STZ诱导的糖尿病小鼠的血清Cr、BUN和UACR水平,缓解肾小球肥大、系膜区扩张和肾纤维化,其治疗效果与足细胞特异性敲除GOLM1相似。机制上,GOLM1中和抗体能有效阻断GOLM1与EGFR的结合,恢复PPARγ/AMPKα通路的活性,进而抑制炎症和氧化损伤。更重要的是,抗体治疗未对小鼠产生任何副作用,血清谷丙转氨酶(ALT)、谷草转氨酶(AST)、肌钙蛋白T、肌酸激酶同工酶(CK-MB)、肌酸激酶(CK)等肝、心、肌肉功能指标均无异常,表明GOLM1中和抗体具有良好的安全性和潜在的临床应用价值。这一结果为糖尿病肾病的临床治疗提供了全新的靶向策略,也让研究人员看到了突破现有治疗瓶颈的希望。
三、研究启示与展望
该研究通过多模型、多技术手段,首次明确了足细胞GOLM1在糖尿病肾病中的致病作用,构建了“GOLM1-EGFR-PPARγ-AMPKα”的调控通路,不仅丰富了糖尿病肾病的发病机制研究,更提供了全新的生物标志物和治疗靶点。对于肾脏疾病研究人员而言,该研究的创新点在于:一是发现了GOLM1在足细胞中的特异性作用,打破了以往对GOLM1在代谢性疾病中作用的认知;二是明确了GOLM1的自分泌调控模式,为靶向分泌型分子的治疗提供了新思路;三是验证了GOLM1中和抗体的治疗效果,为临床转化奠定了基础。
未来,研究人员可进一步探索GOLM1在糖尿病肾病不同分期中的表达变化,明确其作为生物标志物的临床诊断价值;同时,可深入优化GOLM1中和抗体的给药方式和剂量,推进其临床转化研究。此外,该研究中发现GOLM1的GAP活性与其调控糖尿病肾病的功能无关,这一现象背后的原因仍需进一步探究,有望为GOLM1的功能研究提供新的方向。
参考文献
Xu P, Li K, Liu H, Xu A, Zhang Z, Yang Y, Lai X, Hao K, Fang K, Lai Z, Ou X, Cai Y, Wang Z, Lu K, Jiang W. Inhibition of AMPKα Pathway by Podocyte GOLM1 Exacerbates Diabetic Nephrology in Mice. Adv Sci (Weinh). 2025 Oct;12(37):e05695. doi: 10.1002/advs.202505695. Epub 2025 Jul 13. PMID: 40652516; PMCID: PMC12499477.
EnkiLife恩玑生命产品:
