RAW264.7细胞是一种广泛使用的鼠源性单核巨噬细胞系,最初由Abelson白血病病毒诱导的小鼠白血病细胞分化而来。其来源为BALB/c小鼠的单核细胞或巨噬细胞。形态上,RAW264.7细胞具有典型的巨噬细胞特征,呈现圆形或不规则形状,能够贴壁生长,并在适宜条件下表现出明显的伪足结构,方便其进行吞噬作用。RAW264.7细胞在生物医学研究中具有广泛的应用,由于其来源于巨噬细胞,这些细胞在研究免疫反应、炎症机制、破骨细胞分化研究等方面具有重要的模型作用。

- RAW264.7细胞通常会同时呈现出两种细胞形态:单核细胞(梭形)+巨噬细胞(圆形)。细胞生长密度越大时,巨噬细胞(圆细胞)就会越多,所以一般建议高密度培养,密度达到90-100%时进行传代。
- 在正常培养条件下,未经诱导分化的RAW264.7细胞形态上呈现松散贴壁的梭形和圆形。当细胞密度较大时,部分细胞会脱落漂浮,这些漂浮的细胞是存活的,在传代时应收集起来,300-500g离心3-5分钟,细胞沉淀重悬后可以继续培养。
- 由于RAW264.7细胞容易发生分化,因此不建议使用胰酶消化细胞,以避免诱导不必要的分化反应。传代时,可吸走大部分培养液,留下少许培养液(例如使用T25培养瓶则留下2-3 ml左右),用移液器吹散贴壁细胞,待大部分细胞脱落,轻柔吹打混匀制成单细胞悬液,按照合适的比例进行传代或者接板。
- RAW264.7细胞对血清质量非常敏感,低质量的血清可能引起细胞贴壁能力变化或者细胞分化,应选用高质量的胎牛血清。
脂多糖(Lipopolysaccharide, LPS)诱导的RAW264.7炎症模型是研究巨噬细胞介导炎症反应的金标准体外模型。LPS作为革兰氏阴性菌外膜的主要成分,能够被细胞表面的Toll样受体4(TLR4)识别,通过激活下游级联信号通路,触发促炎介质的大量释放。这一模型因其操作简便、反应稳定、机制清晰的特点,被广泛应用于炎症机制研究和抗炎药物的初步筛选。
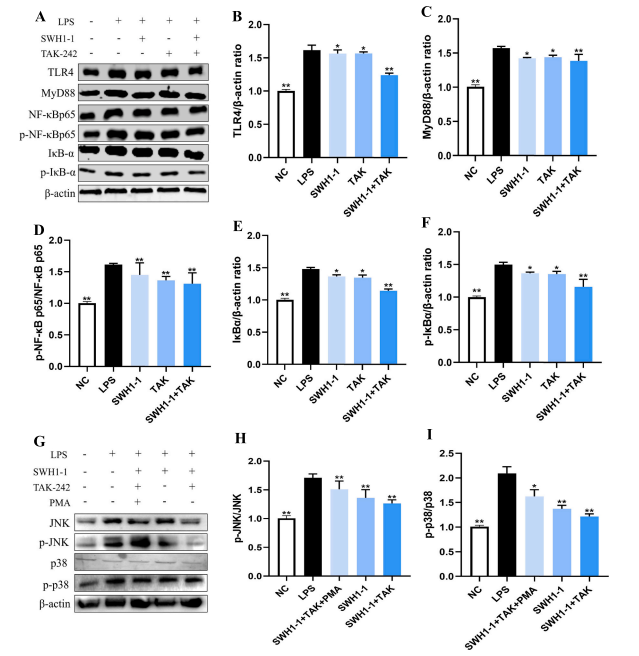
Xianqun Meng[1]等人利用体内LPS诱导的急性肺损伤(ALI)小鼠模型和体外LPS诱导的RAW264.7巨噬细胞研究了接骨木根多糖(SWH1-1)的抗炎潜力。在这项研究中,RAW264.7细胞被用作急性炎症的体外模型。研究人员首先使用脂多糖(LPS)处理RAW264.7细胞,诱导其激活为促炎表型,模拟急性肺损伤状态下肺泡巨噬细胞的过度炎症反应。随后,将纯化的接骨木根多糖SWH1-1与激活的RAW264.7细胞共培养。SWH1-1处理后,研究人员通过生化检测发现,RAW264.7细胞的炎症状态发生显著改变:炎症介质一氧化氮(NO)的产生明显减少,而促炎因子肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)和白细胞介素-1β(IL-1β)的分泌水平显著下调。WB结果进一步揭示(图2),SWH1-1通过抑制TLR4/NF-κB/MAPK信号通路的激活,有效阻断了LPS诱导的炎症级联反应。这表明SWH1-1具有显著的体外抗炎活性,为其作为治疗急性肺损伤的潜在抗炎候选药物提供了实验依据。
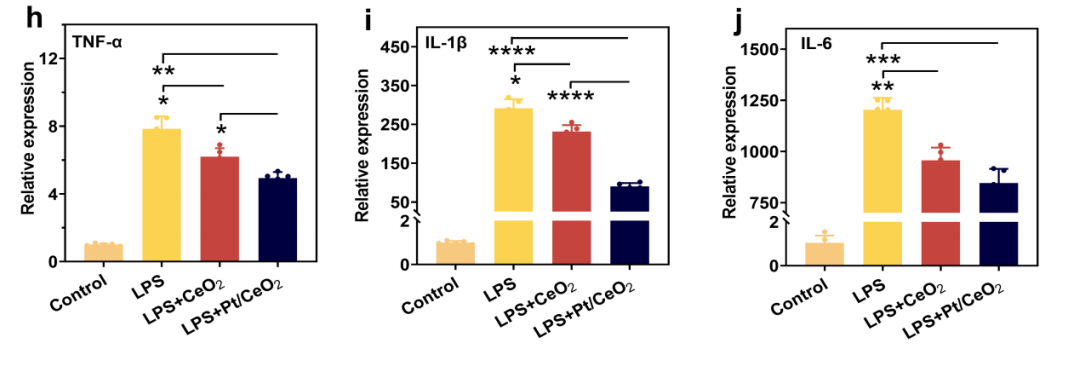
Jian Zhao[2]等人利用体内LPS诱导的角膜炎小鼠模型和体外LPS刺激的RAW264.7巨噬细胞研究了单原子铂掺杂纳米氧化铈(single-atom Pt/CeO₂)的抗炎活性和角膜修复潜力。研究人员首先使用脂多糖(LPS)刺激RAW264.7细胞,诱导其激活为促炎表型,模拟角膜炎等炎症性疾病中免疫细胞的过度激活状态。随后,将合成的单原子铂掺杂纳米氧化铈(single-atom Pt/CeO₂)与激活的RAW264.7细胞共培养。single-atom Pt/CeO₂处理后,研究人员通过qRT-PCR检测发现,RAW264.7细胞的炎症因子表达发生显著改变:促炎细胞因子白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)和肿瘤坏死因子-α(TNF-α)的mRNA水平明显下调,较LPS刺激组降低约50%-70%(n≥3, P<0.05)(图3)。这表明single-atom Pt/CeO₂有效抑制了LPS诱导的RAW264.7细胞炎症反应。
巨噬细胞的功能可塑性是其参与免疫调节的核心特征。根据微环境中的刺激信号不同,巨噬细胞可向两个功能相反的方向极化:促炎的M1型(经典激活型)和抗炎的M2型(选择性激活型)。RAW264.7细胞因其良好的极化响应性,成为研究巨噬细胞功能转换机制的理想模型。
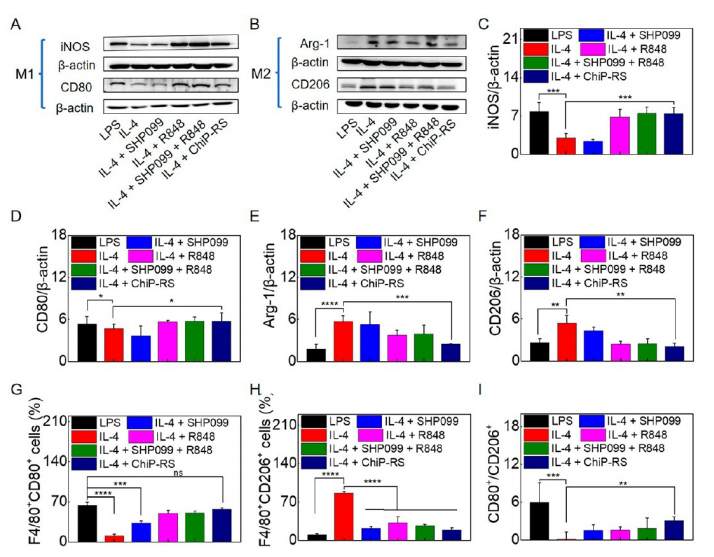
XiaYun Chen[3]等人构建嵌合肽工程生物调节剂(ChiP-RS),通过靶向TAMs将M2型巨噬细胞重极化为M1型,恢复吞噬功能,激活T细胞抗肿瘤免疫。在这项研究中,RAW264.7细胞被用作肿瘤相关巨噬细胞(TAMs)的体外模型。研究人员首先使用IL-4(20 ng/mL)处理RAW264.7细胞24小时,诱导其极化为M2型巨噬细胞,模拟肿瘤微环境中免疫抑制的巨噬细胞表型。随后,将构建的嵌合肽工程生物调节剂(ChiP-RS)与M2型RAW264.7细胞共培养。ChiP-RS处理后,研究人员通过流式细胞术检测发现(图4),RAW264.7细胞的表型发生显著改变:M2型标志物CD206的表达明显下调,而M1型标志物CD86和诱导型一氧化氮合酶(iNOS)的表达显著上调。这表明RAW264.7细胞从促肿瘤的M2表型逆转为抗肿瘤的M1表型。进一步的功能实验显示,重极化后的RAW264.7细胞对肿瘤细胞(4T1乳腺癌细胞)的吞噬能力显著恢复。机制研究通过Western blot证实,ChiP-RS通过激活NF-κB信号通路并抑制STAT6磷酸化,驱动巨噬细胞表型转换。
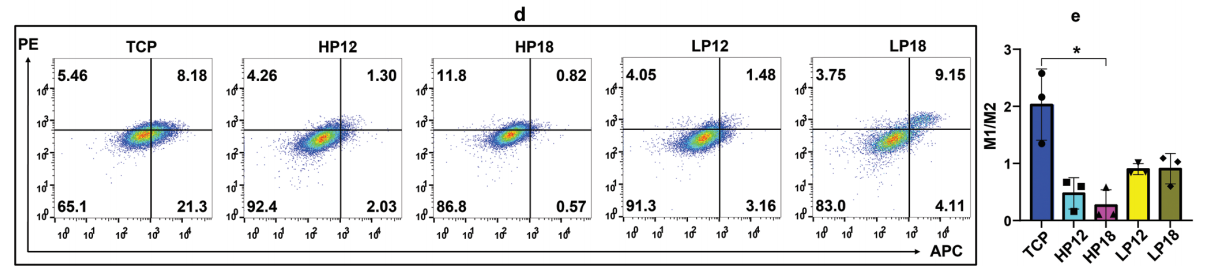
Yajun Shuai[4]等人利用体内巴马猪大段骨缺损模型和体外RAW264.7巨噬细胞研究了取向性皮质骨样丝素蛋白层状支架的骨再生能力和免疫调节潜力。该研究利用RAW264.7细胞评估新型生物材料的免疫调节活性。研究人员将RAW264.7细胞与定向皮质骨样丝蛋白层材料直接共培养,观察材料对巨噬细胞行为的影响。通过流式细胞术检测巨噬细胞表型标志物发现,M1型促炎表型标志物CD86表达显著下调,M2型抗炎表型标志物CD206表达明显上调,实验结果显示,这种仿生骨结构能够显著促进RAW264.7细胞向M2型抗炎表型极化(图5)。此外,研究人员还利用RAW264.7细胞的破骨分化潜能,在RANKL诱导下评估材料对破骨细胞形成的影响。结果显示,该材料能够有效抑制过度活跃的破骨分化,维持骨代谢平衡。这些体外实验结果表明,定向皮质骨样结构通过调控RAW264.7细胞向M2型极化,创造有利于骨再生的抗炎微环境,从而促进间充质干细胞的成骨分化,最终加速大段骨缺损的修复。
RAW264.7细胞在核因子κB受体活化因子配体(Receptor Activator of Nuclear Factor-κB Ligand, RANKL)的诱导下,可分化为具有骨吸收功能的成熟破骨细胞。这一特性使其成为研究骨质疏松症、类风湿关节炎、牙周病及肿瘤骨转移等骨代谢疾病的核心体外模型。
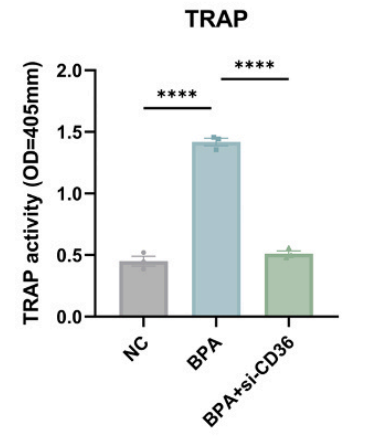
Wenhao Wang[5]等人利用体内大鼠下颌骨缺损模型和体外RANKL诱导的RAW264.7巨噬细胞研究了BPA/DBP通过CD36介导的外泌体信号通路促进破骨细胞分化的分子机制。在这项研究中,RAW264.7细胞被用作破骨细胞分化的体外模型。研究人员首先使用50 ng/mL RANKL处理RAW264.7细胞,诱导其向破骨细胞方向分化,模拟骨吸收过程中的关键细胞类型。随后,将BPA处理的BMSC来源外泌体与RAW264.7细胞共培养。BPA-BMSC外泌体处理后,研究人员通过Western blot检测发现,RAW264.7细胞的破骨细胞标志物发生显著改变:RANKL和NFATC1蛋白表达水平明显上调,而CD36敲低组(BPA+si-CD36)来源的外泌体则显著降低了这些标志物的表达。这表明BPA通过上调BMSC中CD36的表达,改变了外泌体的cargo组成,进而促进RAW264.7细胞向破骨细胞表型分化。进一步的功能实验显示,经BPA外泌体处理的RAW264.7细胞表现出显著增强的TRAP(酒石酸抗性酸性磷酸酶)活性,这是破骨细胞功能成熟的关键指标(图6)。
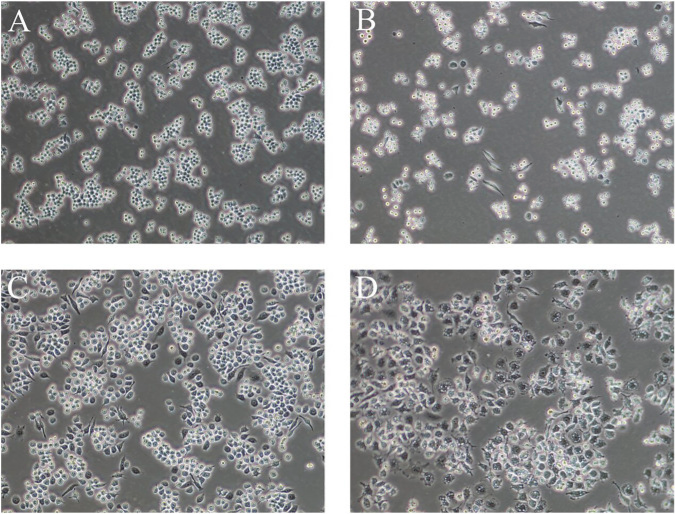
- 细胞铺板:取细胞状态良好的RAW264.7细胞,用细胞血球计数板进行计数,并调整细胞密度为5×10⁴~1×10⁵个/mL,接种至96孔板,每孔100 μL,放入细胞培养箱孵育过夜,使细胞完全贴壁。
- LPS诱导:吸弃原来的培养基,将培养基更换为无血清或低血清(1%FBS)DMEM培养基,置于37℃、5%CO₂培养2~4 h。设置实验组别,其中对照组不加LPS,只加等量培养基;实验组加入不同浓度LPS,如0.1 μg/mL、1 μg/mL、10 μg/mL等,同时每个浓度设置3~4个复孔,并根据不同实验要求继续培养4~24 h,例如早期炎症因子检测可选择6 h。
- 检测指标:
- 细胞活力:若细胞接种于96孔板可用CCK-8或者MTT法检测经不同LPS浓度诱导后,检测RAW264.7细胞的活力,进一步筛选出LPS诱导炎症模型的最佳浓度。
- NO的释放:按照NO检测试剂盒说明书,收集6孔板细胞培养上清通过Griess试剂检测经LPS处理后NO的释放情况。
- 炎症因子分泌:收集6孔板细胞培养上清,按照ELISA试剂盒说明书操作,检测TNF-α、IL-6等炎症因子含量。
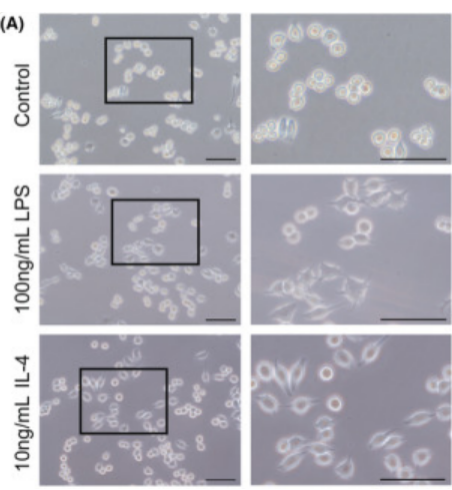
M1极化诱导实验步骤
- 取对数生长期的RAW264.7细胞,消化后用完全培养基调整细胞浓度至5×10⁵个/mL;
- 将细胞悬液均匀接种到6孔板中,每孔2 mL,置于培养箱中培养24小时,待细胞贴壁且融合度达50%-60%;
- 取出培养24 h的细胞板,弃去孔内旧的完全培养基;
- 配置诱导培养基:完全培养基中加入重组小鼠IFN-γ(20 ng/mL)和LPS(100 ng/mL)[7],轻柔混匀;
- 实验分组:对照组(完全培养基)和诱导组(IFN-γ+LPS),每组3复孔;
- 细胞板摇匀后放回培养箱37℃、5%CO₂持续培养24-48 h(优选48 h)。
M1型巨噬细胞极化鉴定:形态观察(M1组细胞体积增大,伪足增多)及标志物检测(ELISA检测TNF-α、IL-6,WB检测iNOS)。
M2极化诱导实验步骤
- 取对数生长期RAW264.7细胞调整浓度至5×10⁵个/mL,接种6孔板培养24h;
- 实验分组:对照组和IL-4诱导组(含终浓度20 ng/mL IL-4)[3];
- 两组继续培养48小时诱导M2极化。
M2型巨噬细胞极化鉴定:形态学观察(M2呈梭形/纺锤形)、流式细胞检测CD206阳性比例升高、Arg-1活性增强。
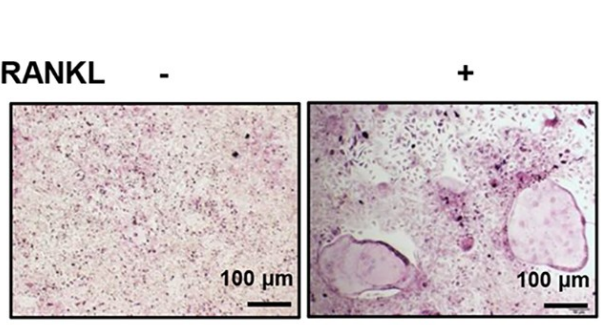
- RAW264.7细胞铺板:用移液器轻轻吹下细胞(无需胰酶消化),接种3000-5000个细胞每孔到24孔板中,500 μL/孔;
- 约4h细胞贴壁后,加入含30 ng/mL RANKL和50 ng/mL M-CSF[9]的DMEM完全培养基,每孔500 μL;
- 隔天换液,诱导5-7天观察,可见多核、有伪足的破骨细胞,TRAP染色鉴定(胞浆红紫色)。
[1] Meng X, Wei Q, Wang S, et al. Anti-inflammatory effect of polysaccharides from Sambucus williamsii Hance roots in lipopolysaccharide-stimulated RAW264.7 macrophages and acute lung injury in mice. Int J Biol Macromol. 2025;306(Pt 1):141368.
[2] Zhao J, Lou W, Wang Y, et al. Single-atom Pt doped nanoceria for enhanced cell phagocytosis and nanozyme activities in keratitis immune regulation. J Nanobiotechnology. 2026;24(1):145.
[3] Chen XY, Yan MY, Liu Q, Yu BX, Cen Y, Li SY. Chimeric Peptide Engineered Bioregulator for Metastatic Tumor Immunotherapy through Macrophage Polarization and Phagocytosis Restoration. ACS Nano. 2023;17(16):16056-16068.
[4] Shuai Y, Yang T, Zheng M, et al. Oriented Cortical-Bone-Like Silk Protein Lamellae Effectively Repair Large Segmental Bone Defects in Pigs. Adv Mater. 2025;37(10):e2414543.
[5] Wang W, Ma A, Zhai C, et al. Bisphenol A and Di-n-butyl phthalate disrupt bone homeostasis bidirectionally via CD36-mediated BMSCs autophagy inhibition and exosome-promoted osteoclastogenesis. J Hazard Mater. 2025;497:139703.
[6] Huang J, Chen R, Zhou J, et al. Comparative pharmacokinetic study of the five anti-inflammatory active ingredients of Inula cappa in a normal and an LPS-induced inflammatory cell model. Front Pharmacol. 2022;13:981112.
[7] Sun C, Zhao X, Wang X, et al. Astragalus Polysaccharide Mitigates Rhabdomyolysis-Induced Acute Kidney Injury via Inhibition of M1 Macrophage Polarization and the cGAS-STING Pathway. J Inflamm Res. 2024;17:11505-11527.
[8] Li J, Ren H, Zhang Z, Zhang J, Wei F. Macrophage M2 polarization promotes pulpal inflammation resolution during orthodontic tooth movement. J Cell Mol Med. 2024;28(9):e18350.
[9] Zhi X, Wang L, Chen H, et al. l-tetrahydropalmatine suppresses osteoclastogenesis in vivo and in vitro via blocking RANK-TRAF6 interactions and inhibiting NF-κB and MAPK pathways. J Cell Mol Med. 2020;24(1):785-798.
[10] Xue Y, Zhao C, Liu T. Interferon-induced protein with tetratricopeptide repeats 1 (IFIT1) accelerates osteoclast formation by regulating signal transducer and activator of transcription 3 (STAT3) signalling. Bioengineered. 2022;13(2):2285-2295.
 | Flora Flora是EnkiLife的技术支持专家,熟悉免疫学和神经科学,致力于为客户提供高品质的产品搭配和技术支持,以帮助实现神经退行性疾病和其它神经科学方面的研究。 |
文档内容完全忠实于原始资料 · RAW264.7细胞培养与应用参考
