文献分享:胃癌空间分辨图谱揭示淋巴细胞聚集区的关键作用
一、研究背景
胃癌作为全球范围内高发的消化道恶性肿瘤,其发病率和死亡率居高不下,临床治疗中仍面临晚期患者预后差、免疫治疗应答率不均等突出问题,而肿瘤微环境的复杂特性正是影响治疗效果和患者生存的关键因素之一。研究已证实,肿瘤微环境并非单一的肿瘤细胞集合,而是由免疫细胞、非免疫细胞及细胞外基质共同构成的复杂生态系统,其细胞组成及其空间分布会直接影响癌症患者的临床结局,尤其是免疫细胞的分布与功能状态,更是决定抗肿瘤免疫应答效率的核心。尽管单细胞RNA测序(scRNA-seq)技术的发展,已为解析多种癌症的免疫细胞组成提供了有力工具,能够精准识别不同类型的免疫细胞亚型,但该技术无法捕捉细胞在组织内的空间位置信息,导致淋巴细胞的空间分布模式,尤其是三级淋巴结构(TLSs)对其分布的影响仍不明确。三级淋巴结构作为肿瘤微环境中淋巴细胞的重要聚集位点,其存在与否、成熟程度与多种癌症患者的预后密切相关,却因缺乏空间维度的研究,其调控淋巴细胞分布、参与抗肿瘤免疫的具体机制尚未被完全阐明。同时,以往基于单细胞测序数据推断肿瘤微环境中细胞间相互作用的研究,多依赖基因表达的计算机模拟预测,缺乏基于配体和受体空间共现的原位探索,导致细胞间通讯的实际发生场景和调控机制难以精准解析。此外,T细胞亚群,尤其是作为预后评估和免疫治疗反应关键指标的耗竭T细胞,其在肿瘤微环境中的空间分布特征、活化机制及与其他细胞的相互作用,也尚未得到深入研究。基于以上研究空白和临床需求,《A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region》一文中,聚焦肿瘤微环境(TME)这一癌症免疫治疗的核心靶点,通过整合单细胞转录组学和空间转录组学技术,构建胃癌的空间分辨细胞图谱,旨在系统揭示肿瘤微环境的空间组织特征、三级淋巴结构的核心作用及免疫检查点分子的空间分布规律,为胃癌免疫治疗生物标志物的探索提供新视角,为临床个体化免疫治疗策略的制定提供科学依据。
二、研究方法
该研究招募了27名未接受过治疗的胃癌患者,收集其手术切除肿瘤、组织学正常的邻近组织、淋巴结和外周血四种组织样本,通过单细胞RNA测序获得470,609个单细胞的转录组数据,同时对19个肿瘤样本进行33张空间转录组(ST)切片分析,覆盖肿瘤核心、中间区域和边缘三种采样位置,获得61,035个ST斑点数据。首先构建高分辨率单细胞图谱,识别出8种主要细胞类型及53种细胞亚型,利用BBKNN消除平台批次效应,通过Leiden算法进行聚类分析,随后结合RCTD方法整合单细胞和空间转录组数据,将ST斑点聚类为四个空间区域,结合H&E染色图像验证区域合理性并命名。通过基因集富集分析(GSEA)探究各空间区域的信号通路活性,利用多重免疫组织化学(mIHC)验证关键细胞亚型和分子的表达,结合TCGA数据库进行生存分析,借助RedeHist算法进行细胞核分割和基因表达推断,系统分析细胞亚群的空间分布、细胞间相互作用及与临床表型的关联。
三、结果分析
肿瘤微环境中细胞亚型的空间分布
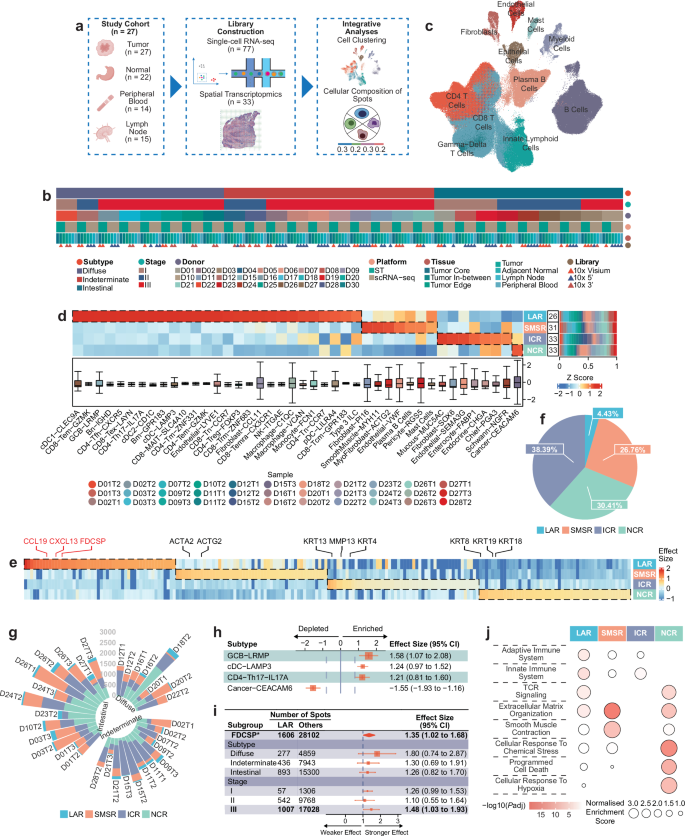
为搭建整个研究的基础框架,明确肿瘤微环境的细胞组成与空间特征,研究首先清晰呈现了完整研究流程,即从27名胃癌患者收集四种组织样本,分别进行单细胞RNA测序和空间转录组分析,再通过整合分析构建空间分辨图谱,同时展示四种组织的核心信息,为后续组织特异性分析提供参考。研究通过对470,609个单细胞进行UMAP投影分析并按主要细胞类型进行颜色编码,成功识别出T细胞、B细胞、髓系细胞等免疫细胞,以及内皮细胞、基质细胞、上皮细胞等非免疫细胞共8种主要细胞类型,且每种细胞类型均通过经典基因标志物验证,确保了细胞分型的准确性。为进一步明确细胞亚型的空间分布规律,研究采用RCTD方法获得各细胞亚型在不同空间区域的富集得分热图(按z分数归一化),结合堆叠条形图展示各空间区域在所有ST样本中的占比,通过箱线图呈现各细胞亚型在61,035个斑点中的富集得分分布,最终成功识别出四个具有独特细胞亚型组成的空间区域,同时发现淋巴细胞亚型的富集得分偏差较小,而非淋巴细胞亚型偏差较大,推测这一现象与淋巴细胞在肿瘤组织中的迁移特性密切相关。为给各空间区域的功能定位提供分子依据,研究筛选出各区域的差异表达基因并绘制热图,发现其中一个区域高表达淋巴节点相关基因CXCL13、CCL19等,另一个区域高表达平滑肌相关基因ACTA2、ACTG2等。此外,研究还统计了所有ST样本中四个空间区域的占比,发现淋巴细胞聚集相关区域占比最低;同时按胃癌亚型分组,呈现每个ST样本中各空间区域的占比,揭示了不同亚型胃癌的空间区域分布差异。为明确淋巴细胞聚集区域的免疫特征,研究通过森林图分析该区域中富集和耗竭的细胞亚型,以效应量0.8和-0.8为临界值,发现GCB-LRMP、cDC-LAMP3等免疫细胞在该区域显著富集,而Cancer-CEACAM6细胞显著耗竭,明确了该区域的免疫优势特征。研究还通过森林图分析FDCSP基因表达与临床表型的关联,发现其与III期胃癌的关联更为显著;通过气泡图展示各空间区域富集的独特信号通路,例如淋巴细胞聚集区域富集适应性和先天性免疫系统相关通路,平滑肌相关区域富集平滑肌收缩相关通路,缺氧相关区域富集细胞缺氧反应相关通路,直接将空间区域与功能特性关联起来。
LAR区域中初始 CD8+T 细胞的活化启动
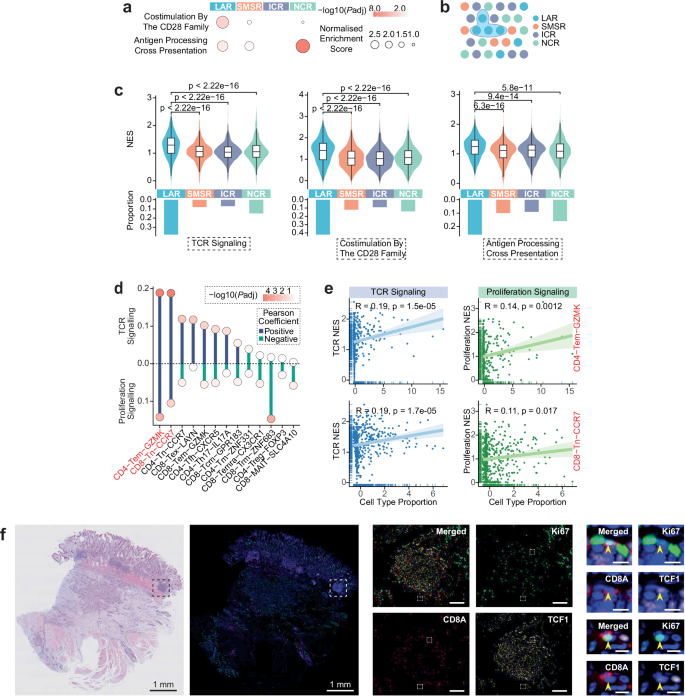
为探究淋巴细胞聚集区(LAR)的核心功能,研究聚焦T细胞激活过程,从信号通路、细胞关联及实验验证三个层面展开系统分析。为明确不同空间区域的T细胞激活潜力,研究通过气泡图展示了T细胞激活相关信号通路在各空间区域的强度,发现LAR区域中CD28家族共刺激、抗原加工交叉呈递等关键通路信号显著增强,为T细胞激活提供了坚实的分子证据。为实现区域内的精细分析,研究定义空间块为同一ST分组、空间上相邻的斑点集合,以此作为后续研究单元。为进一步验证LAR区域在T细胞激活中的核心作用,研究通过小提琴图和条形图结合的方式,对比各空间区域T细胞激活关键通路的标准化富集得分(NES)及富集该通路的斑点比例,证实LAR区域的T细胞激活通路强度和激活斑点比例均显著高于其他区域。为筛选出与T细胞激活相关的关键T细胞亚群,研究通过棒棒糖图展示了T细胞亚群丰度与两种T细胞激活相关通路的Pearson相关系数及统计显著性,进一步聚焦CD4-Tem-GZMK和CD8-Tn-CCR7两种亚群,通过散点图呈现其细胞丰度与TCR、增殖信号通路的具体关联,发现两者均与两种通路呈正相关,且相关性具有统计显著性,提示这两种T细胞亚群可能在LAR区域被激活。为从蛋白水平验证这一激活现象,研究采用mIHC染色技术,观察特定样本中CD8A、TCF1、Ki67三种分子的表达,通过全切片视图、LAR区域放大视图及更高倍镜视图,清晰观察到LAR区域中存在TCF1+KI67+CD8A+细胞,且这一现象在主要研究队列的11个样本和独立验证队列的5个样本中均有发现,为LAR区域的免疫激活功能提供了直接实验证据。
LAR的发育谱系与其抗肿瘤免疫的关联
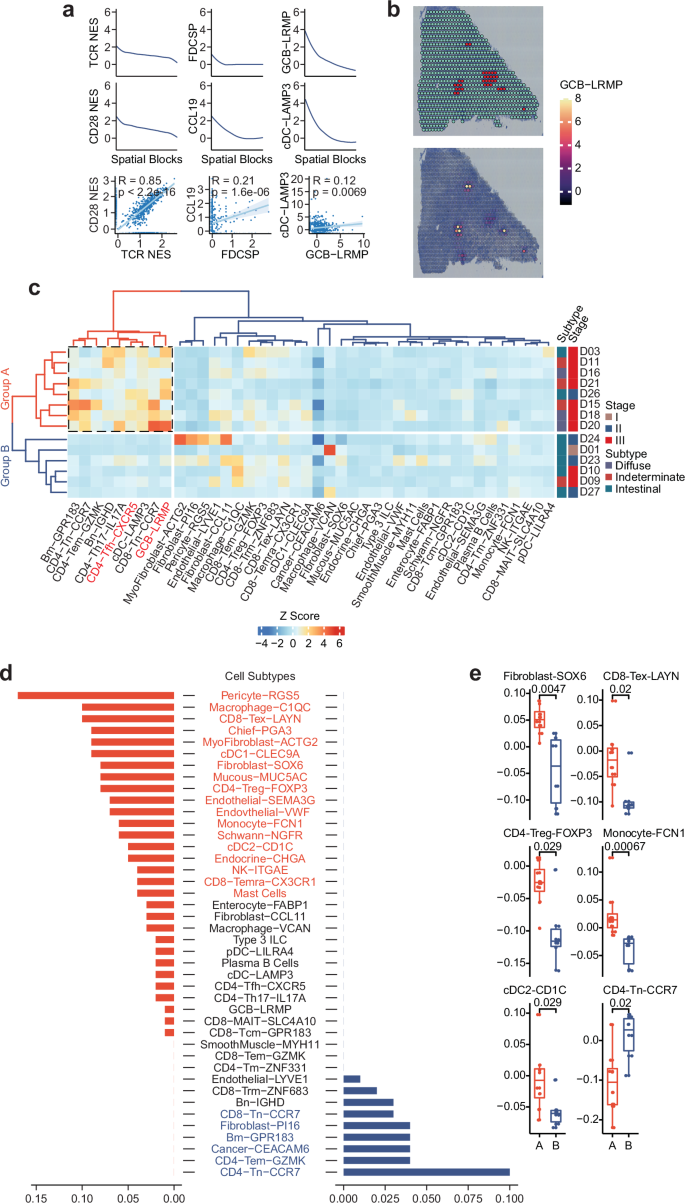
为深入解析淋巴细胞聚集区的异质性及其对肿瘤微环境中淋巴细胞分布的影响,研究展开了系列针对性分析。为探究LAR区域功能指标的协同性,研究通过线图展示了T细胞激活相关信号通路、基因标志物(FDCSP、CCL19)及细胞亚型(GCB-LRMP、cDC-LAMP3)在不同LAR空间块中的表达趋势,同时通过散点图呈现各指标间的关联,发现TCR信号通路与CD28信号通路、CCL19与FDCSP、GCB-LRMP与cDC-LAMP3均呈显著正相关。为验证LAR区域的内部异质性,研究将特定样本的H&E图像与GCB-LRMP细胞丰度进行叠加分析,以红色标记LAR区域,用颜色密度表示细胞丰度差异,结果发现即使在单个样本的LAR块中,GCB-LRMP细胞丰度也存在明显异质性。为进一步探究LAR异质性对肿瘤微环境的影响,研究通过z分数转换的LAR区域斑点细胞组成,将患者分为A、B两组,发现A组患者多为III期,其LAR块中高表达淋巴结富集的细胞亚型,如GCB-LRMP、CD4-Tfh-CXCR5,而B组患者的LAR块中此类细胞信号较弱。为明确两组患者癌性区域的淋巴细胞分布差异,研究通过热图展示A、B两组患者在癌性区域中各细胞亚型的丰度差异,发现A组中激活型淋巴细胞,如CD8-Tex-LAYN、CD4-Treg-FOXP3丰度显著高于B组,而B组中静息型淋巴细胞,如CD4-Tn-CCR7、CD8-Tn-CCR7丰度显著高于A组。随后通过箱线图对比16名A组患者和10名B组患者的关键细胞亚型丰度差异,进一步验证了这一分布差异,最终揭示了不同LAR亚群对肿瘤微环境中淋巴细胞分布的调控作用——A组LAR相邻癌性区域聚集激活型淋巴细胞,B组则聚集静息型淋巴细胞。
肿瘤中免疫检查点分子的空间分布模式
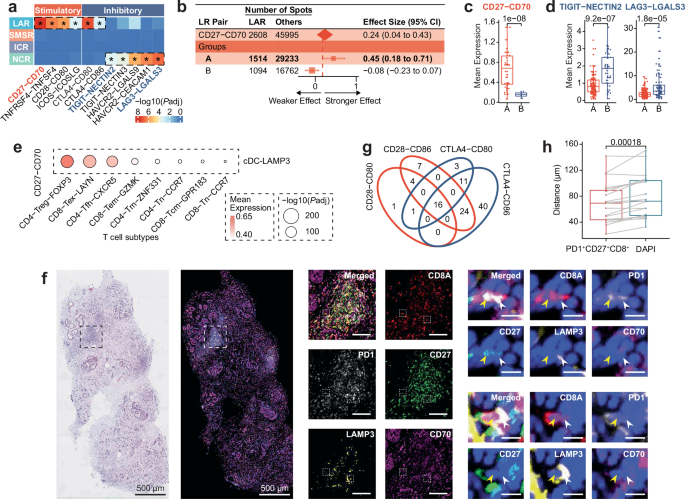
为挖掘潜在的免疫治疗靶点,研究围绕免疫检查点配体-受体对的空间分布展开系统探究,明确其空间特异性特征。研究首先分析不同空间区域中富集的免疫检查点配体-受体对,发现淋巴细胞聚集区显著富集刺激性配体-受体对,尤其是CD27-CD70,缺氧相关区域显著富集抑制性配体-受体对,如LAG3-LGALS3、TIGIT-NECTIN2,而平滑肌相关区域和另一种癌性区域未出现明显的配体-受体对富集。为探究CD27-CD70这一刺激性轴与患者分组的关联,研究通过森林图呈现其与A、B两组患者的关系,发现该轴在A组LAR块中的表达显著高于B组,随后通过箱线图直接对比两组LAR块中CD27-CD70的表达水平,进一步验证了该刺激性轴在A组LAR中的优势表达。同时,研究通过箱线图对比A、B两组NCR块中抑制性轴,LAG3-LGALS3和TIGIT-NECTIN2的表达水平,发现B组NCR块中抑制性轴表达更高,结合B组癌性区域Cancer-CEACAM6细胞丰度更高的特点,推测癌性细胞可能参与抑制性轴的表达调控。为明确CD27-CD70轴的细胞来源,研究基于单细胞RNA测序数据,通过气泡图分析推断,cDC-LAMP3 细胞与 CD4-Treg-FOXP3、CD8-Tex-LAYN 等 T 细胞亚群可通过该轴实现细胞间通讯。为从原位水平验证这一细胞间相互作用,研究采用mIHC染色技术,观察特定样本中CD8A、PD1、CD27、LAMP3、CD70的表达,通过不同放大倍数的视图,清晰观察到LAR区域中PD1+CD27+CD8+细胞与CD70+LAMP3+细胞的物理接触,且这一现象在主要队列和独立验证队列中均有发现。为探究LAR区域中免疫检查点分子的平衡状态,研究通过韦恩图展示同时表达CD28和CTLA4相关轴的LAR空间块,发现此类块主要集中在A组,提示A组LAR区域中可能存在CD28与CTLA4竞争结合CD80/CD86的平衡状态。最后,研究通过箱线图对比LAR区域中PD1+CD27+CD8+细胞与CD70+LAMP3+细胞的平均距离,以及DAPI与CD70+LAMP3+细胞的平均距离,发现前者显著更短,进一步证实了两种细胞的近距离相互作用,为CD27-CD70轴介导的T细胞激活提供了有力的空间证据。
四、研究结论与意义
该研究通过整合单细胞和空间转录组学技术,成功构建了胃癌的高分辨率空间分辨细胞图谱,识别出四个具有独特转录组特征的空间区域(LAR、SMSR、ICR、NCR),其中LAR区域作为淋巴细胞聚集区,包含淋巴细胞聚集体和三级淋巴结构,在T细胞激活、淋巴细胞分布调控及免疫检查点分子表达中发挥关键作用。研究发现,LAR区域中初始 T细胞丰度与T细胞激活相关通路显著关联,且LAR存在异质性,可分为A、B两组,分别对应癌性区域中激活型和静息型淋巴细胞的聚集;同时,LAR区域富集CD27-CD70等刺激性免疫检查点轴,A组LAR中PD1+CD27+CD8 T细胞与CD70+LAMP3+树突状细胞近距离聚集,为T细胞激活提供了空间和分子基础。该研究不仅揭示了胃癌肿瘤微环境的空间组织特征,还为免疫治疗生物标志物的筛选提供了新靶点,为胃癌免疫治疗的个体化策略制定提供了重要参考,同时其整合单细胞与空间转录组学的研究方法,也为其他癌症的肿瘤微环境研究提供了借鉴。
参考文献
Gao S, Qin S, Wang D, Wang A, Zhu L, Li Y, Shi Q, Fan H, Bo Y, Zhong Y, Sun Y, Dong K, Fu L, Gao R, Wu Y, Liang Y, Huang L, Hu X, Ren X, Bu Z, Ji J, Zhang Z. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun. 2026 Jan 27;17(1):2059. doi: 10.1038/s41467-026-68612-z. PMID: 41593079; PMCID: PMC12948980.
EnkiLife mIF 技术服务
提供有偿代检和分析服务
承接多色配套服务
分类 | 服务项目 | 备注 |
|---|---|---|
IHC染色 | IHC单色标记 | |
IF荧光染色 | 免疫荧光单标 | 不含一抗,含二抗(兔/小鼠/大鼠)、DAPI。 四标以上染色需要提供多余白片做单标预实验。 |
荧光多标染色 | ||
全景扫描 | 免疫组化全景扫描 | 提供读片软件及原始相关文件,荧光扫描波长范围。 |
荧光标记全景扫描 | ||
数据分析 | 免疫组化及免疫荧光切片分析 | 可进行全片单阳性、多阳性细胞数及面积分析,也可定制分析特征病理区域,或进行空间分析、位置分析等。 |
