文献分享:多重免疫荧光与传统组织学联合成像用于肿瘤生物标志物发现
一、研究背景
肿瘤微环境的精准解析是癌症诊断、预后评估及治疗决策的核心基础,而传统组织成像技术存在明显局限:单一免疫荧光(IF)成像虽能检测多分子标志物,但缺乏组织形态学背景支撑,难以准确定位细胞类型及分布。苏木精-伊红(H&E)染色作为病理诊断金标准,可清晰呈现组织形态,却无法提供分子水平的免疫特征信息。现有多重成像技术要么流程复杂、耗时较长,要么存在荧光串扰、试剂稳定性不足等问题,难以实现分子标志物+组织形态的同步精准检测。
针对这一痛点,研究团队开发了一个结合了H&E形态学知识和高重分子信息的全玻片成像平台,实现对同一细胞的多维度检测。结直肠癌(CRC)作为常见恶性肿瘤,其预后评估依赖于肿瘤内在特征和免疫浸润水平,但传统免疫评分存在参数单一、预测效能有限等不足。本研究旨在验证Orion技术的可靠性、重复性,并基于该技术开发更精准的结直肠癌预后评估模型,为临床转化提供实验依据。
二、研究方法
本研究围绕Orion多模态组织成像技术的验证、优化及临床应用展开,核心涵盖技术体系构建与验证、实验样本与数据采集、数据分析与模型构建三个环节。
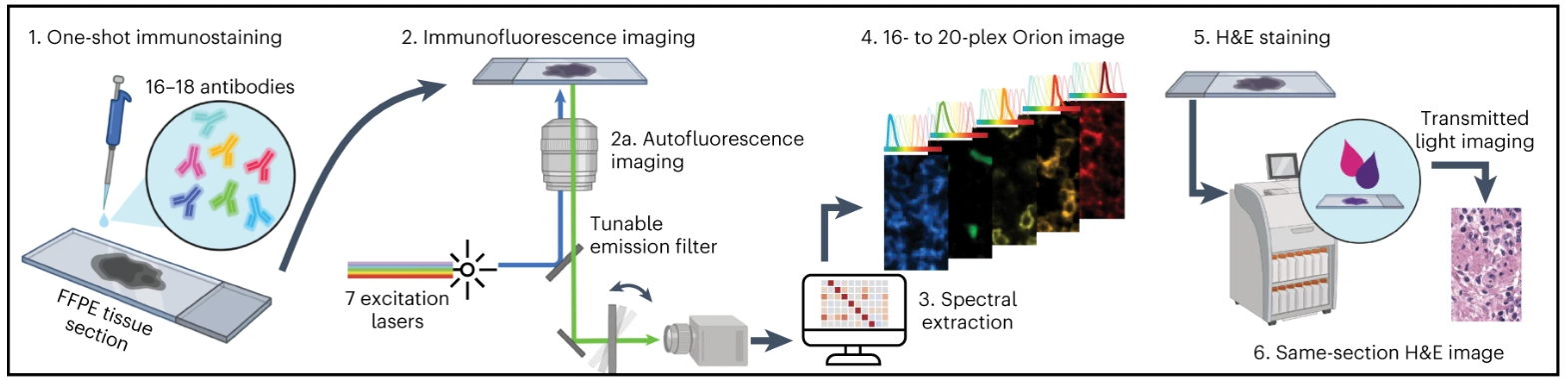
多重免疫荧光染色的实验设计与核心流程围绕Orion技术的适配性、可行性和可重复性展开,首先设计构建适用于上皮性肿瘤及其癌旁正常组织微环境研究的抗体面板,涵盖免疫细胞标志物、上皮细胞标志物、内皮细胞标志物及功能标志物,同时通过与传统免疫组化染色结果比对完成抗体验证,检测相邻通道荧光串扰并验证光谱提取技术对串扰的抑制效果,确保串扰率降至1%以下。染色与成像核心流程聚焦解决H&E与IF兼容问题,先准备FFPE组织切片,包括扁桃体、肺癌、CRC组织及组织芯片TMA,进行单次16-18种ArgoFluor偶联一抗的Orion多重IF染色并完成成像,之后使用工业标准切片染色机进行H&E染色,经病理学家评估确认达到诊断级质量,最后通过Orion成像系统获取全切片图像并结合软件完成光谱提取、细胞分割等数据分析。为验证方法的有效性、可重复性和实用性,实验设置三组核心分组,分别为用于验证抗体面板适用性的扁桃体、肺癌组织验证组,用于验证方法广泛适用性的含30种正常/非肿瘤疾病组织及18种肿瘤组织的TMA组,以及用于预后标志物筛选和模型构建的74例I-IV期CRC切除标本队列组,其中6例标本在两个不同实验室进行重复实验以验证跨实验室的可重复性。
三、结果分析
多重荧光成像的可行性及通道串情况
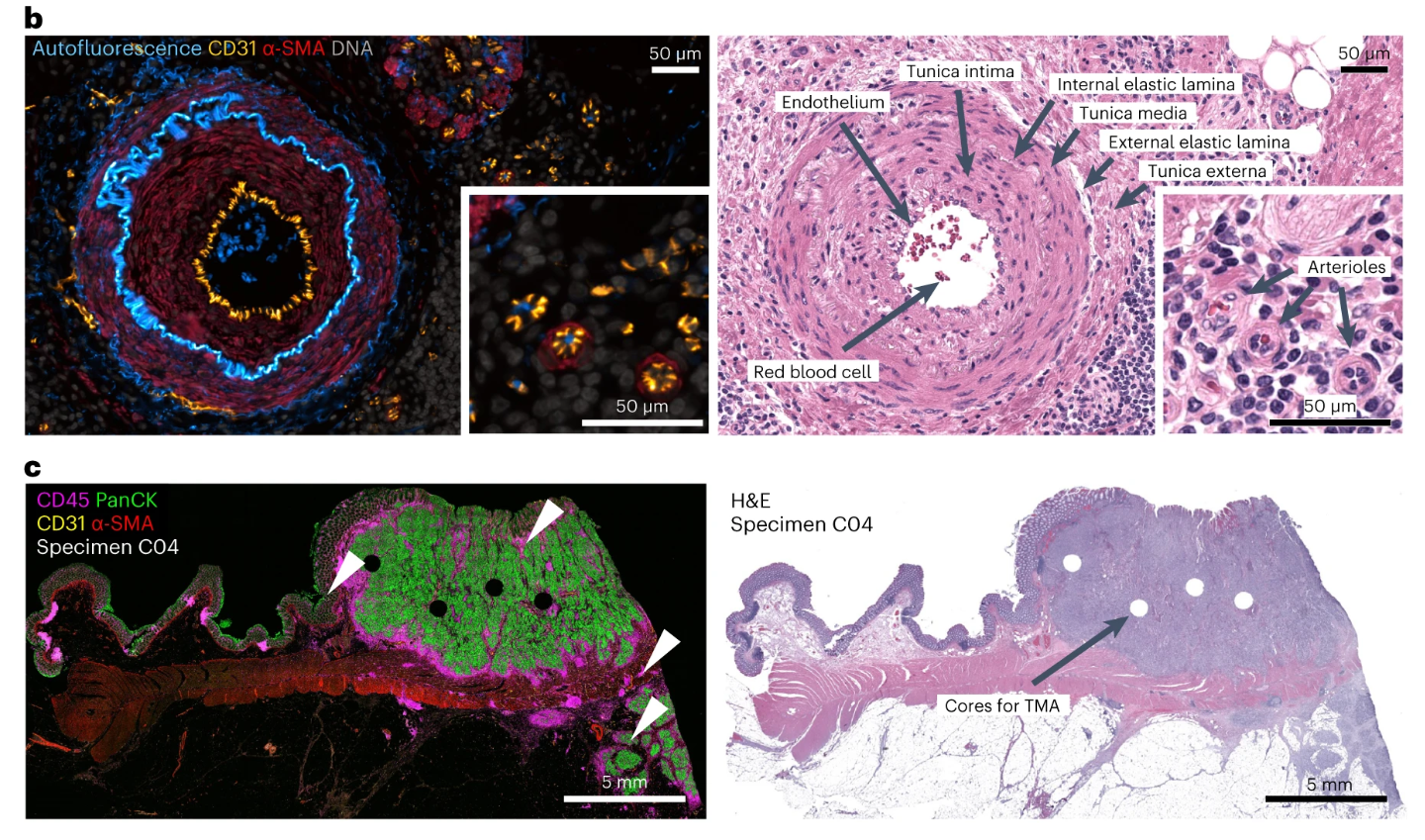
研究从不同维度系统验证了Orion多重荧光成像技术的基础性能,为后续所有实验的开展提供了核心技术支撑。图中通过自发荧光通道与IF抗体通道的叠加成像,不仅清晰呈现了组织内结缔组织、血管等天然荧光结构的分布特征,还能有效突出目标生物标志物的特异性荧光信号,直观印证了自发荧光通道在提升生物标志物信噪比、减少背景干扰方面的重要作用,确保后续标志物检测的准确性。
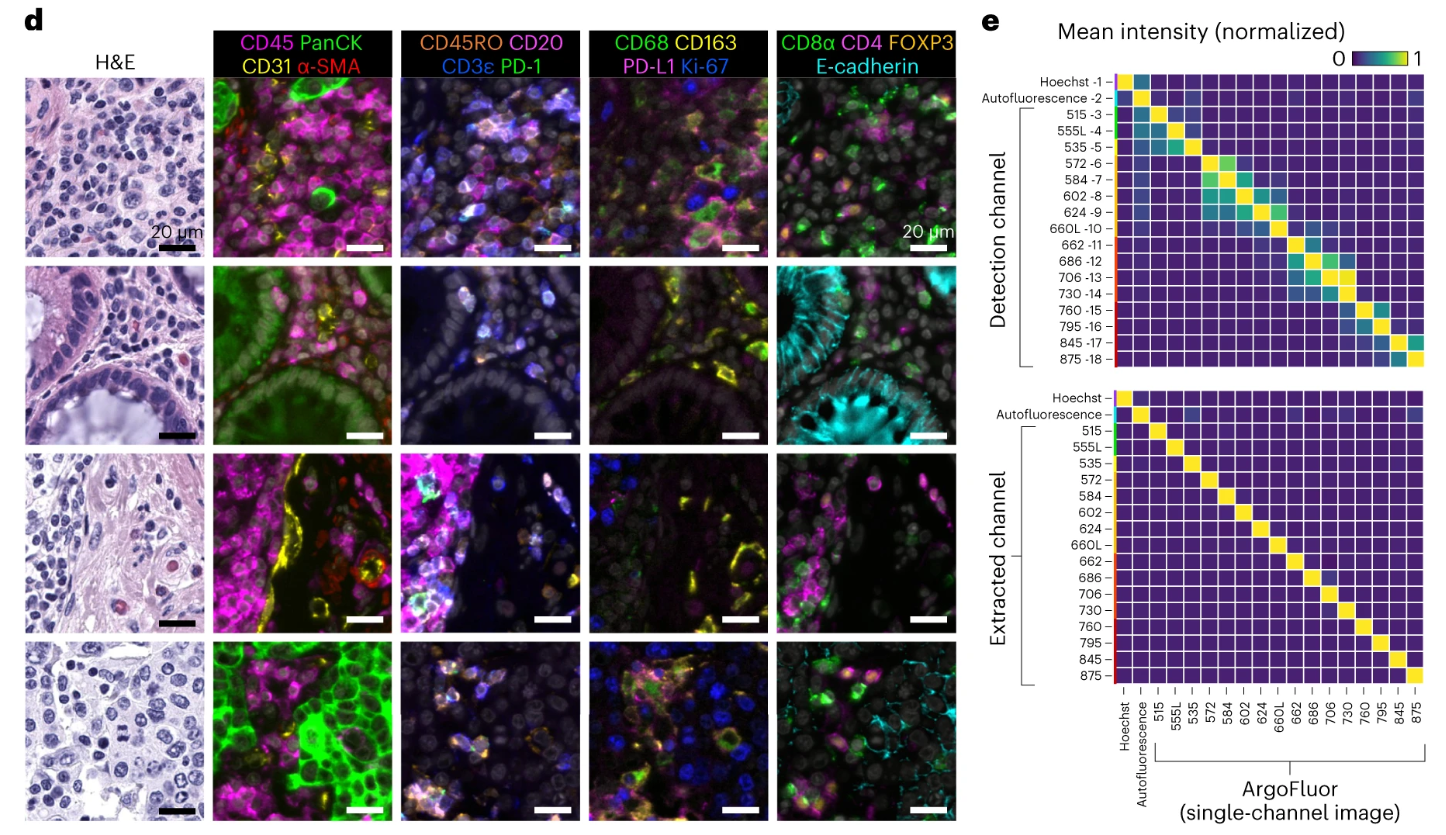
图d的单图高分辨率成像细节,可清晰呈现细胞轮廓、细胞核及细胞膜上目标标志物的荧光染色情况,甚至能分辨亚细胞水平的荧光分布,充分满足后续细胞分型、亚细胞定位等精细化分析的需求。图e通过定量分析明确了光谱提取技术的显著效果,实验中通过单抗体标记扁桃体组织,检测相邻荧光通道的串扰情况,结果显示未进行光谱提取时,相邻通道串扰平均约为35%,易导致不同抗体的荧光信号混淆,而经过光谱提取处理后,串扰率降至<1%,成功解决了多重荧光成像中通道串扰这一核心技术痛点,为单轮18-20重、循环32重的高plex成像提供了可靠的技术保障,确保每一种抗体的荧光信号都能被准确识别和量化。
多重荧光成像展示
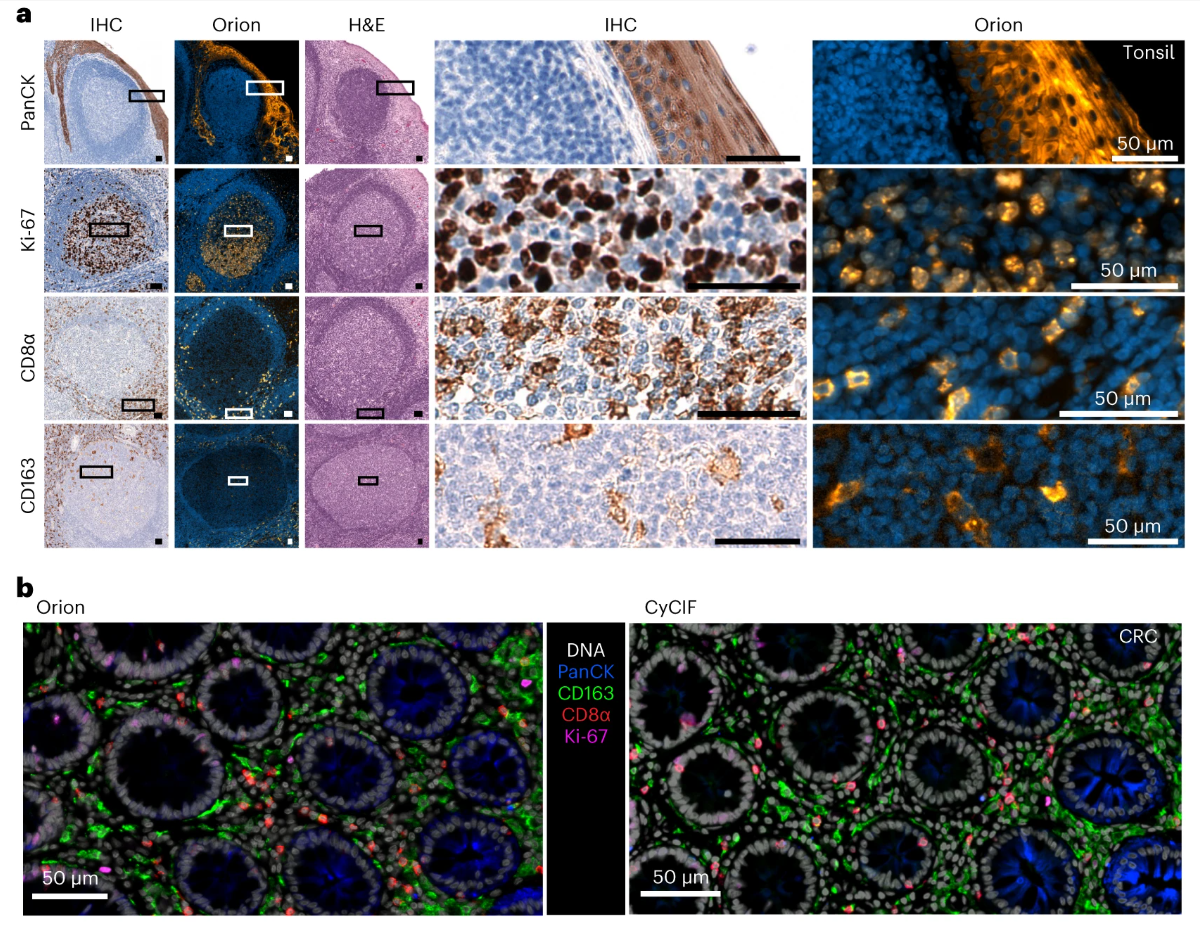
通过多维度对比实验,全面验证了Orion多重荧光抗体组合的可靠性、准确性和实用性。研究选取pan-cytokeratin、Ki-67、CD8α、CD163四种核心标志物,对同一扁桃体、肺癌及CRC样本分别进行Orion多重IF与传统IHC染色,结果显示两种方法的染色模式高度相似,如Ki-67主要定位于增殖活跃细胞的细胞核、CD8α主要分布于免疫浸润区域、pan-cytokeratin清晰标记肿瘤细胞轮廓,充分印证了Orion抗体组合的特异性。多重成像质量也不劣于已在领域内验证成熟的CyCIF技术,且本文提出的成像方法的分辨率更具优势,能更好地保留细胞细节信息。
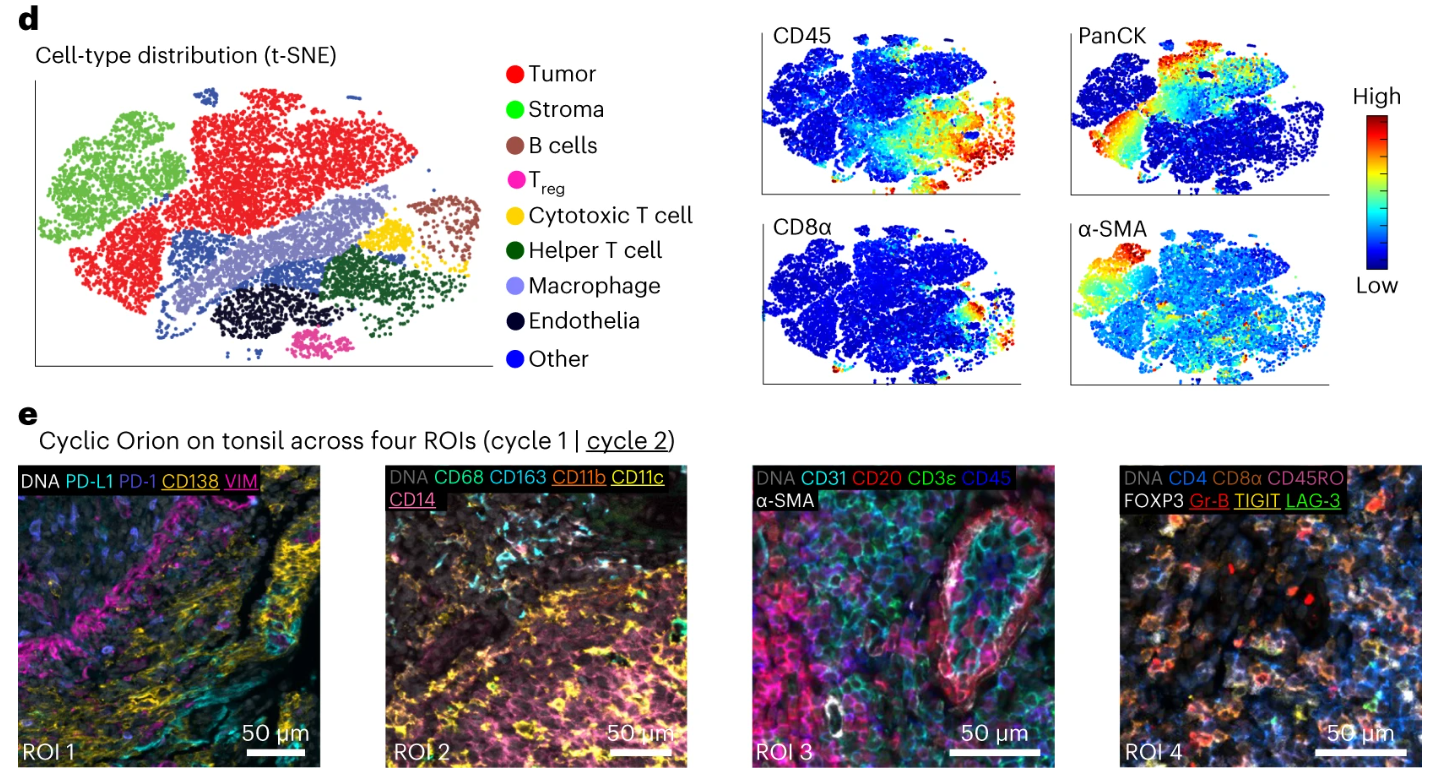
研究基于Orion多重荧光成像获取的18-20重标志物数据,进行t-SNE降维分析,通过算法将高维度的荧光数据降维至二维空间,成功将CRC样本中的肿瘤细胞、免疫细胞、基质细胞等预期细胞群清晰区分,每个细胞群的荧光特征明确,证明Orion多重荧光数据可有效用于细胞分型,为后续细胞水平的深入分析提供了数据基础。之后针对循环Orion成像的可行性进行验证,通过过氧化氢漂白荧光团的方法,实现2轮染色-成像循环,最终获得29种抗体的32重成像数据;实验中量化显示,漂白步骤可使ArgoFluor荧光素的荧光强度降低>95%,轮间串扰处于极低水平,避免了前一轮荧光信号对后一轮成像的干扰。同时,经过2轮IF染色和漂白处理后,样本的HE染色仍保持诊断级质量,可清晰识别组织形态和细胞结构,证实循环成像可有效提升plex数量,且不影响后续组织形态学分析,为更高重数的多重荧光成像提供了可行方案。
IF与HE图像的联合分析
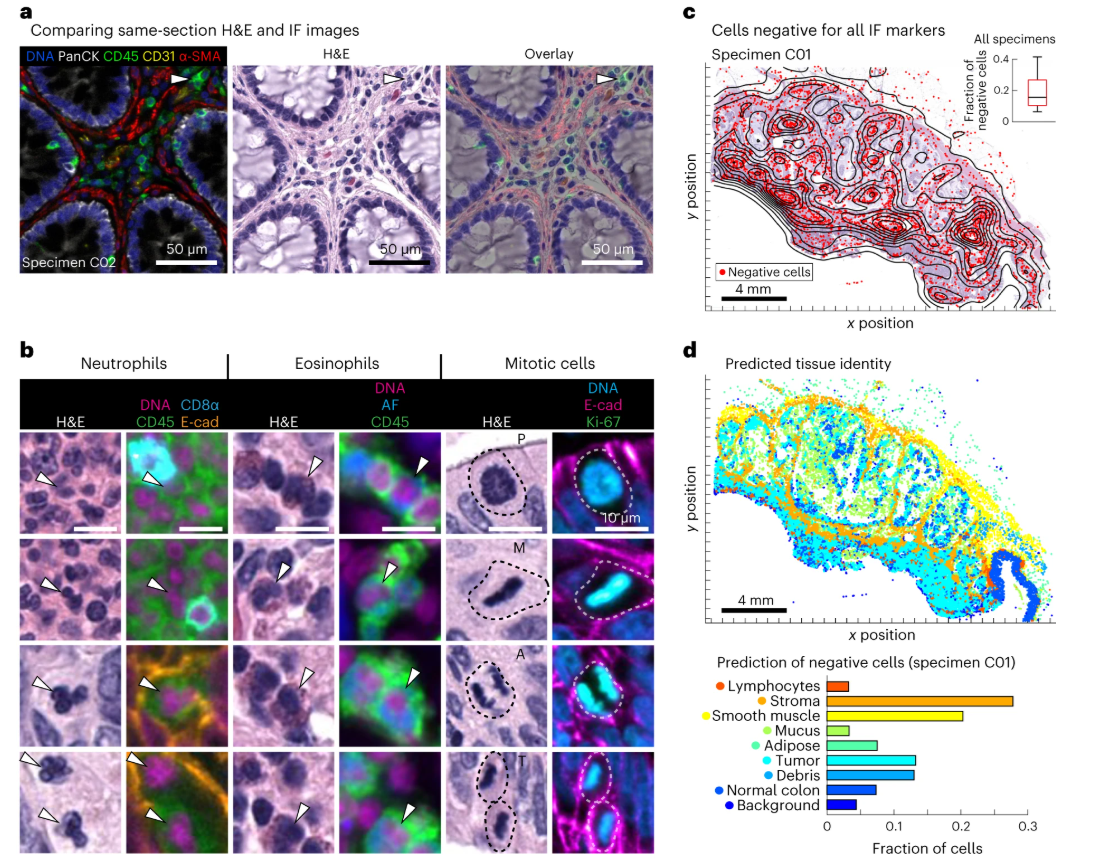
通过多组对比实验,充分验证了两种成像技术的互补性,有效解决了单一成像技术的局限性,显著提升了细胞分型和组织结构识别的准确性。图a选取CRC样本进行IF与HE图像的直接对比,IF成像通过CD4、CD8、CD20等免疫标志物的荧光标记,可清晰区分HE图像中形态相似、难以分辨的免疫细胞亚群,如CD4+ T细胞、CD8+ T细胞和B细胞,这些细胞在HE染色中均呈现为圆形淋巴细胞,无法通过形态学区分,而IF可通过特异性荧光信号精准识别,凸显了IF在细胞分子分型中的独特优势。图b则重点展示了HE染色的形态学优势,HE染色可清晰识别IF中无对应特异性标志物的细胞类型,如嗜酸性粒细胞、中性粒细胞,还能准确分辨细胞有丝分裂的各时期,同时可清晰呈现无细胞结构的组织成分,如基底膜、黏液池等,这些信息均无法通过IF成像获得,有效弥补了IF在形态学分析中的短板。
基于Orion多重IF数据的预后模型构建
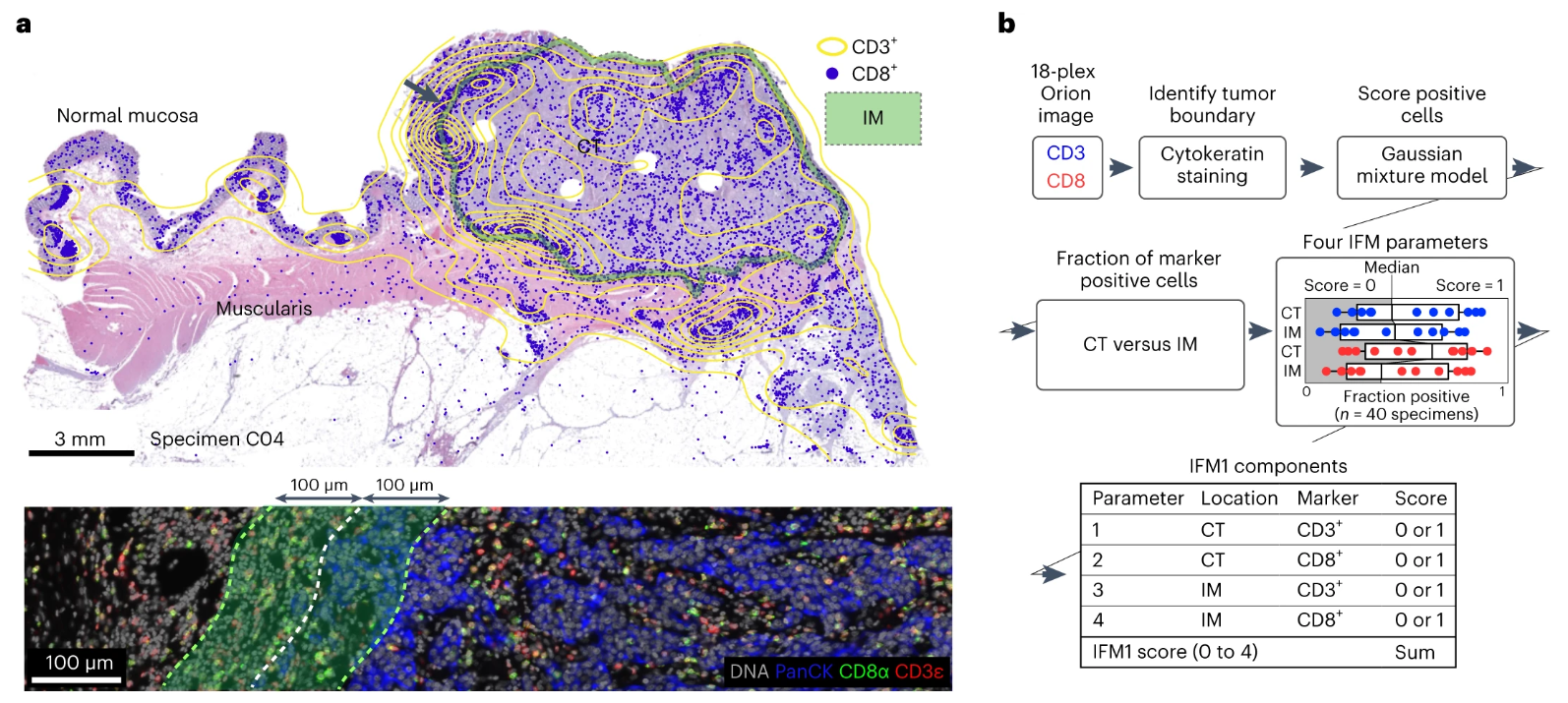
研究通过Orion多重IF成像获取的CD3、CD8等免疫标志物荧光图像,结合自发荧光通道和HE染色图像,清晰定位肿瘤组织与周围基质的边界,精准划分出CT(肿瘤中心)和IM(肿瘤浸润边缘,定义为肿瘤边界±100μm)两个关键区域;其中,肿瘤中心区域以肿瘤细胞为主,免疫细胞浸润较少,而浸润边缘区域为肿瘤细胞与免疫细胞的交界地带,免疫细胞浸润更为丰富,这种精准的区域划分的为后续区域特异性细胞计数提供了可靠的空间基础,确保计数结果的准确性和针对性。图b详细展示了IFM1模型的构建流程,首先通过高斯混合模型对Orion多重IF数据中的CD3+、CD8+细胞荧光信号进行分析,确定两种细胞的阳性阈值,避免因主观判断导致的计数偏差;随后,分别统计CT区域和IM区域的CD3+、CD8+阳性细胞比例,根据比例高低分别赋予0-1分, Orion多重IF数据可高效复刻Immunoscore的预后预测能力,且相比传统Immunoscore需要通过IHC手动计数、操作繁琐、主观性强的缺点,Orion多重IF可实现自动化、高通量的细胞计数,大幅提升了预后评分的效率和客观性。
基于Spatial-LDA的新型预后标志物挖掘
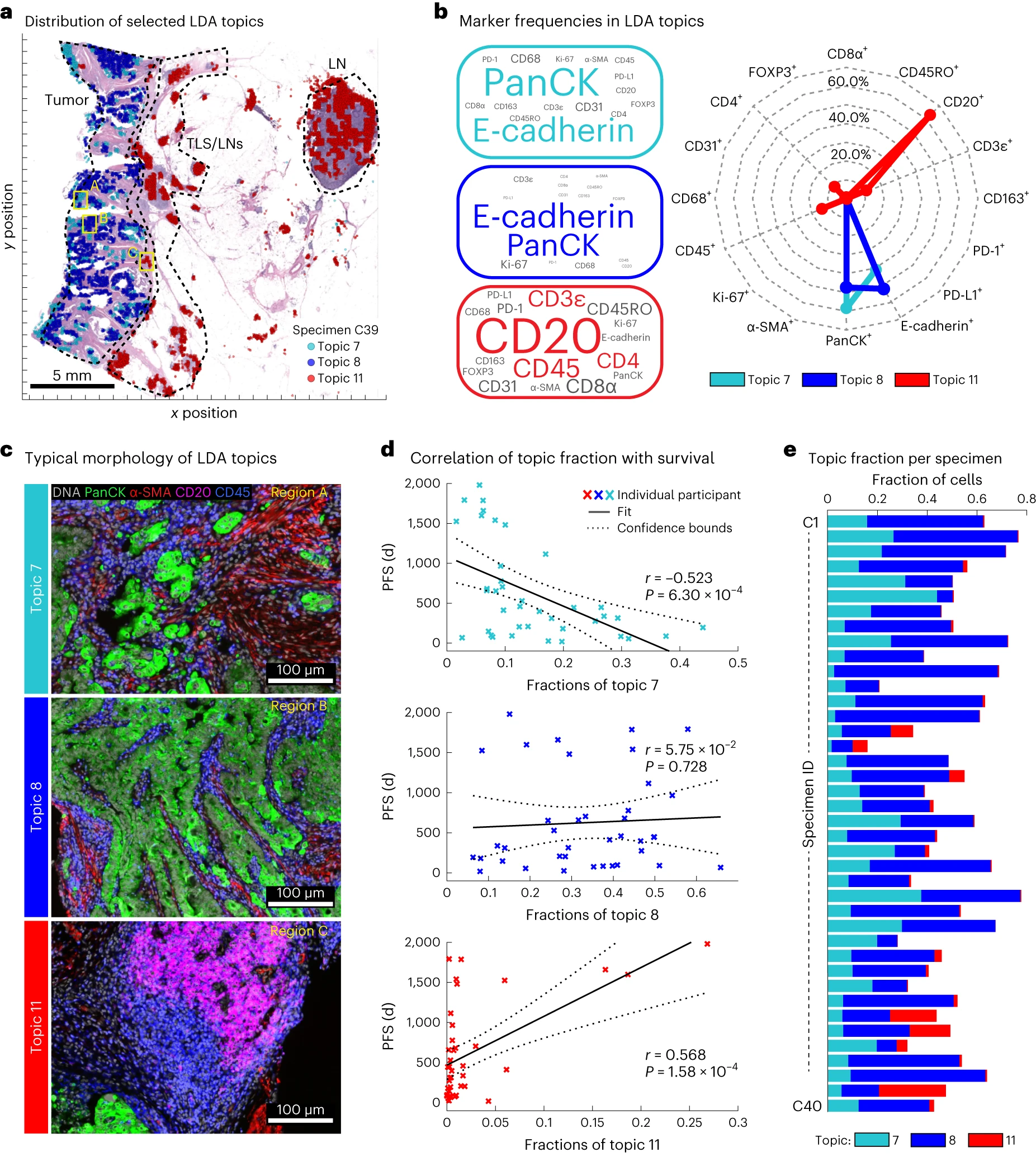
作者采用无偏性的Spatial-LDA算法,对Orion多重IF数据进行深度挖掘,旨在发现与CRC预后相关的新型肿瘤内在特征,避免传统有偏性分析导致的标志物遗漏,为构建更优预后模型提供新的靶点。图a展示了3个代表性空间特征(topics)的空间分布情况,均叠加了HE染色图像以明确组织定位,其中topic7主要分布于肿瘤中心区域,topic11主要分布于肿瘤浸润边缘及淋巴聚集区域,topic8则分散分布于肿瘤间质区域,可见不同topics在肿瘤组织中的空间定位存在显著差异,证明Spatial-LDA算法可有效区分不同的细胞邻里结构和组织区域特征,能够捕捉到传统分析方法难以发现的空间分布差异。图b明确了各topics的标志物组成特征,其中topic7主要由pan-cytokeratin、E-cadherin阳性细胞组成,免疫细胞标志物的贡献极少,提示其主要反映肿瘤细胞自身的特征。topic11主要由CD20阳性细胞组成,CD3、CD4等T细胞标志物有少量贡献,表明其与肿瘤免疫微环境中的B细胞浸润密切相关。topic8与topic7的标志物组成高度相似,均以pan-cytokeratin、E-cadherin阳性细胞为主,但后续分析显示其与预后无相关性,说明并非所有肿瘤细胞相关特征都与预后相关,进一步凸显了无偏性挖掘的必要性。图d通过相关性分析量化了各topics与CRC患者无进展生存期(PFS)的关联,结果显示topic7与PFS呈强负相关,表明topic7比例越高,患者预后越差。topic11与PFS呈强正相关,表明topic11比例越高,患者预后越好。而topic8与PFS无明显相关性,提示topic7是与CRC不良预后密切相关的新型肿瘤内在特征,而topic11则与良好预后相关。图f通过定量统计对比了topic7、8、11的标志物阳性细胞比例,结果显示topic7的pan-cytokeratin+肿瘤细胞比例显著高于topic11,进一步确认了topic7的核心特征为肿瘤细胞相关标志物的高表达,且这种高表达与不良预后直接相关,为后续topic7的深入解读和模型构建提供了明确方向。
四、总结
本文介绍了一种多模态组织成像方法,该方法将单轮、高通量亚细胞分辨率的免疫荧光成像、内源性自发荧光成像与后续同细胞的H&E染色成像相结合,经验证,这种多模态组织成像在不同实验平台间具有良好的可重复性,且对人类观察者和机器学习模型均具有显著优势。通过Orion技术,研究提出了IF与H&E成像的联合使用,其核心价值在于利用H&E的组织显微解剖知识辅助解读分子数据,弥补抗体种类局限,还能表征无细胞结构、区分形态相似但功能不同的细胞。所用Orion仪器支持最多18重同时成像,已在30种组织中验证适用性,可通过循环成像或结合CyCIF增加分子通道。诊断应用中仅需8-14个通道即可降低成本,且H&E能识别多重IF难以分辨的细胞,IF则可辅助区分免疫细胞,二者互补,为临床诊断和科研提供有力工具。基于Orion技术构建的4种预后模型,显著优于传统免疫评分,可精准预测结直肠癌患者的无进展生存期。同时通过Spatial-LDA挖掘出与预后相关的新空间特征,为结直肠癌的预后评估提供了新的思路和标志物。
参考文献
Lin JR, Chen YA, Campton D, Cooper J, Coy S, Yapp C, Tefft JB, McCarty E, Ligon KL, Rodig SJ, Reese S, George T, Santagata S, Sorger PK. High-plex immunofluorescence imaging and traditional histology of the same tissue section for discovering image-based biomarkers. Nat Cancer. 2023 Jul;4(7):1036-1052. doi: 10.1038/s43018-023-00576-1. Epub 2023 Jun 22. PMID: 37349501; PMCID: PMC10368530.
EnkiLife mIF 技术服务
提供有偿代检和分析服务
承接多色配套服务
分类 | 服务项目 | 备注 |
|---|---|---|
IHC染色 | IHC单色标记 | |
IF荧光染色 | 免疫荧光单标 | 不含一抗,含二抗(兔/小鼠/大鼠)、DAPI。 四标以上染色需要提供多余白片做单标预实验。 |
荧光多标染色 | ||
全景扫描 | 免疫组化全景扫描 | 提供读片软件及原始相关文件,荧光扫描波长范围。 |
荧光标记全景扫描 | ||
数据分析 | 免疫组化及免疫荧光切片分析 | 可进行全片单阳性、多阳性细胞数及面积分析,也可定制分析特征病理区域,或进行空间分析、位置分析等。 |
