文献分享:小胶质细胞对阿尔茨海默病脂质代谢的特异性调控
一、研究背景
阿尔茨海默病(AD)作为最常见的神经退行性疾病和痴呆的主要诱因,其核心病理特征之一是大脑稳态的严重紊乱,而脂质代谢异常在疾病进展中的作用长期以来未能得到充分关注。近年来,随着脂质组学技术的发展,研究发现磷脂、鞘脂和胆固醇等脂质的失衡可能是AD发病的始动因素,而非单纯的病理附属产物,这些脂质紊乱可通过调节膜流动性、分泌酶区室化和Aβ聚集动力学等机制推动淀粉样变性。《Microglia-specific regulation of lipid metabolism in Alzheimer’s disease revealed by microglial depletion in 5xFAD Mice》,该研究聚焦大脑常驻免疫细胞——小胶质细胞,结合5xFAD转基因小鼠模型与人类死后脑组织样本,重点探讨小胶质细胞在AD脂质代谢紊乱中的特异性调控作用,旨在破解AD中脂质代谢异常与不同脑细胞类型、分子通路的关联,为疾病治疗提供新的靶点方向。此前研究已证实,小胶质细胞中富集的脂质代谢风险基因(如TREM2、PLCG2、GRN等)参与Aβ清除和神经炎症调控,但小胶质细胞清除对大脑脂质代谢的具体影响却被广泛忽视,仅有一项研究关注到其对白细胞三烯合成的必要性,这也成为本研究的核心切入点。
二、研究方法
该研究以能再现AD淀粉样病理关键特征的5xFAD转基因小鼠为核心模型,涵盖B6SJL和B6两种遗传背景,通过药理学和遗传学两种小胶质细胞耗竭方法,区分AD中依赖小胶质细胞和不依赖小胶质细胞的脂质代谢紊乱机制;药理学耗竭采用CSF1R抑制剂PLX5622,对6周龄5xFAD和正常对照(Non-Tg)小鼠进行短期(2周)和长期(3.5个月)喂食处理,遗传学耗竭则通过将Csf1r增强子缺失小鼠与5xFAD小鼠杂交,获得四种基因型小鼠并在5月龄时取材;研究结合shotgun脂质组学、RNA谱分析(NanoString神经胶质谱分析面板)和免疫荧光技术,检测小鼠大脑中脂质种类、基因表达及病理标志物变化,同时选取10例非疾病对照和10例AD患者的死后脑组织进行脂质组学分析,校正性别和灰白质比例等混杂因素,验证小鼠模型结果的临床相关性,最终通过统计学分析(PLS-DA、火山图、Venn图、相关性分析等)明确小胶质细胞对AD脂质代谢的调控作用及分子机制。
三、结果分析
1、小胶质细胞耗竭策略验证及淀粉样病理表型分析
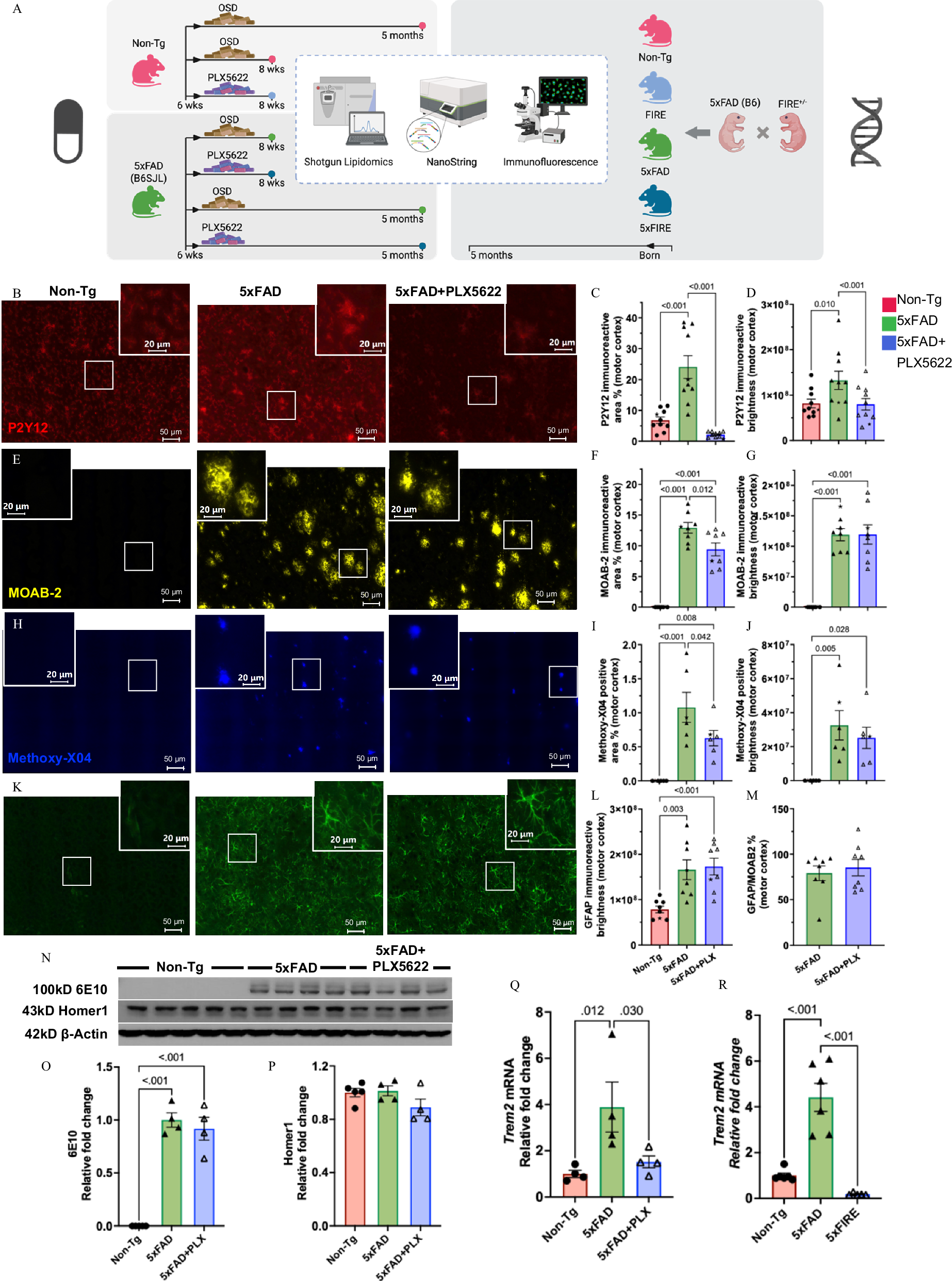
为明确小胶质细胞在AD脂质代谢中的作用,研究首先验证了两种耗竭方法的有效性,并观察其对淀粉样病理的影响。短期PLX5622处理几乎完全清除了5xFAD和Non-Tg小鼠的小胶质细胞,P2Y12免疫反应区减少99%,而长期处理则使5xFAD小鼠的小胶质细胞减少82%,剩余的小胶质细胞多为围绕淀粉样斑块的疾病相关小胶质细胞(DAM),这类细胞的P2Y12免疫荧光强度显著高于非斑块区小胶质细胞,且形态更呈阿米巴样、突起更少。在2月龄时,5xFAD小鼠大脑中几乎无淀粉样沉积物,而5月龄时,其大脑中Aβ和纤维状斑块负荷显著升高,长期PLX5622处理可轻微降低Aβ负荷和纤维状斑块负荷,与此前研究结果一致。值得注意的是,淀粉样变性会显著增加星形胶质细胞的反应性,表现为GFAP免疫反应区和亮度升高,但PLX5622处理并未影响GFAP的强度或免疫反应区(校正Aβ负荷后),也未改变大脑APP蛋白水平和突触密度。遗传学耗竭模型中,5xFIRE小鼠(FIRE与5xFAD杂交后代)的Trem2 mRNA表达几乎检测不到,证实小胶质细胞被有效清除,为后续脂质代谢分析奠定了可靠的模型基础。整个实验设计清晰呈现了小胶质细胞耗竭的动态过程,以及其与淀粉样病理、星形胶质细胞反应性的关联,排除了小胶质细胞耗竭对APP表达和突触密度的直接影响,确保后续脂质代谢变化与小胶质细胞功能的特异性关联。
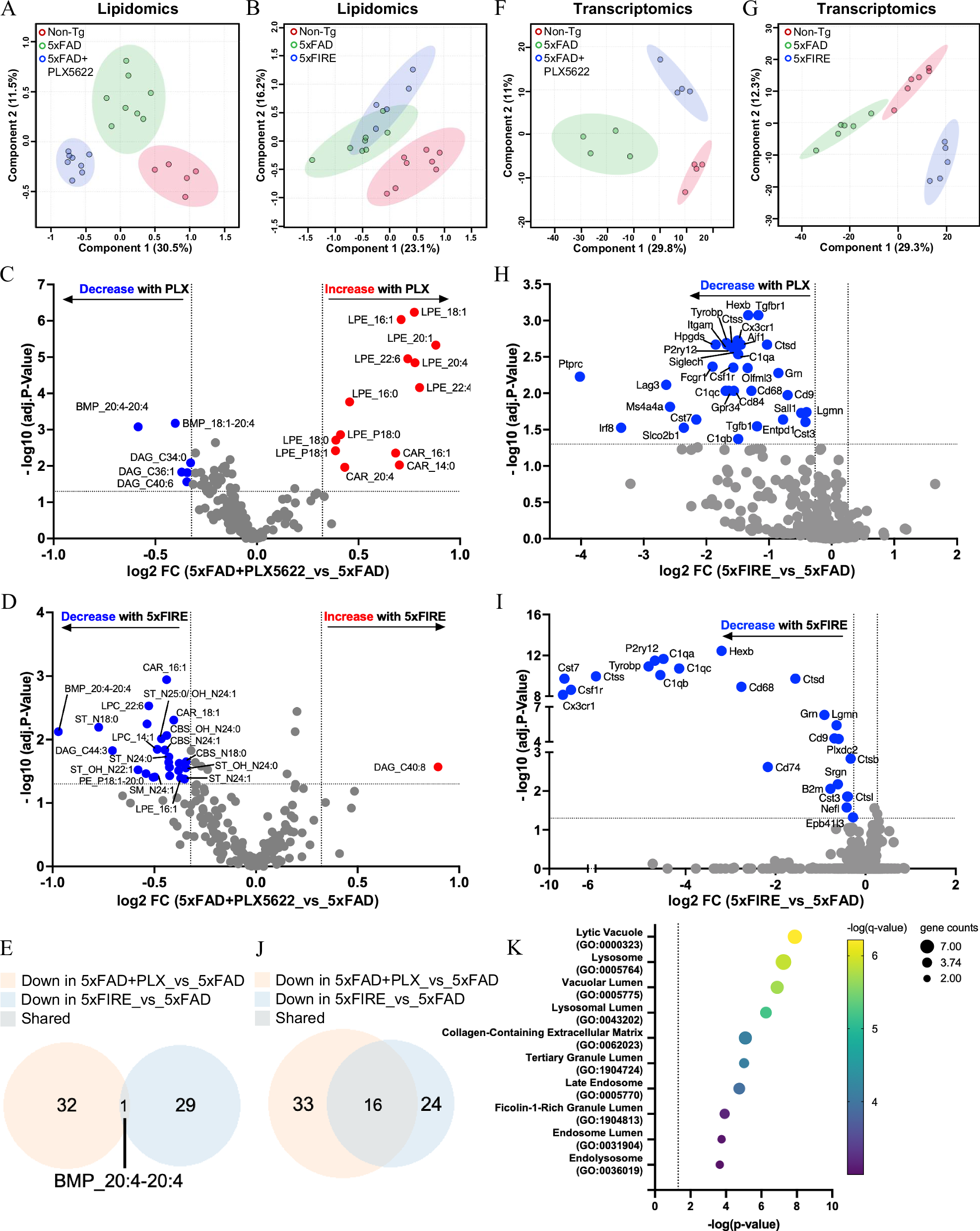
2、淀粉样变性与小胶质细胞耗竭对大脑脂质组和转录组的差异化影响
通过对198种脂质物种的分析,研究发现淀粉样变性会导致大脑脂质组出现显著特征性变化,无论是药理学组还是遗传学耗竭组,Non-Tg与5xFAD小鼠的脂质组都能通过PLS-DA分析清晰区分,且两种队列中均存在LPC、LPE和BMP物种的一致性升高,提示这些脂质与AD淀粉样病理密切相关。更关键的是,小胶质细胞耗竭会引发脂质组的差异化改变:长期药理学耗竭导致脂质组发生更显著的偏移,与5xFAD组形成完全的PLS-DA分离,且显著增加了多种溶血磷脂物种;而遗传学耗竭则独特地降低了髓鞘脂质和能量代谢相关脂质,提示不同耗竭程度对大脑脂质代谢的影响存在差异。但两种耗竭方法存在一个共同的关键发现——均能阻止含花生四烯酸(20:4)的双单酰甘油磷酸(AA-BMP)的积累,这一现象暗示AABMP的积累高度依赖小胶质细胞。转录组分析进一步佐证了这一结论,两种队列中各组的转录组均能通过PLS-DA清晰区分,5xFIRE小鼠的转录组与Non-Tg小鼠的差异比5xFAD小鼠更大,提示完全耗竭小胶质细胞会引发更显著的转录组重塑。淀粉样变性诱导的炎症相关基因在两种队列中均被小胶质细胞耗竭下调,且遗传学耗竭的下调幅度更显著;Venn分析发现,两种耗竭方法共同下调的16个基因均与溶酶体调控相关,结合脂质组学中AABMP与溶酶体通路的关联,进一步揭示小胶质细胞通过调控溶酶体功能参与AD脂质代谢紊乱,为后续AABMP的深入分析提供了分子层面的支撑。
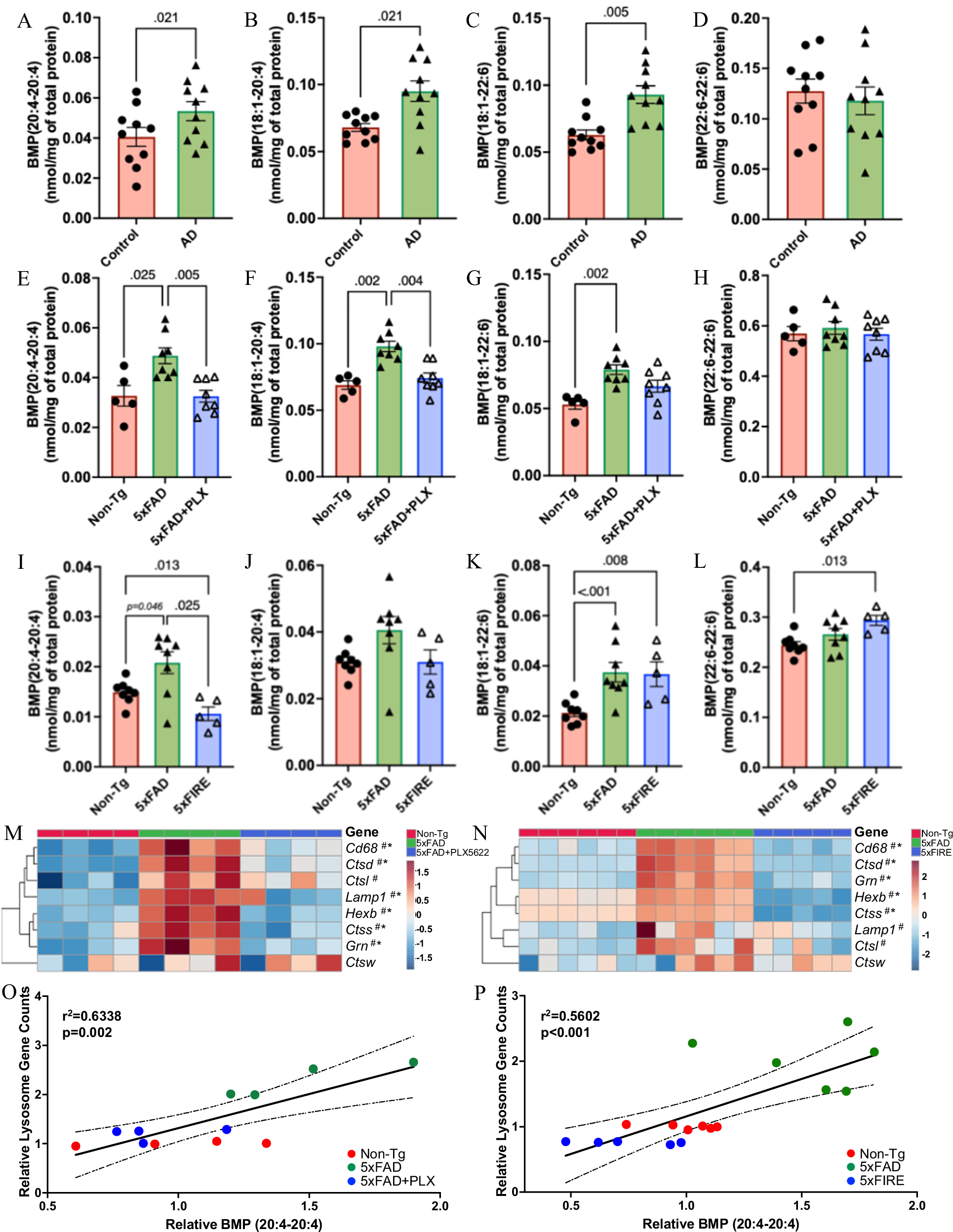
3、小胶质细胞耗竭可阻止淀粉样变性诱导的溶酶体AA-BMP积累
鉴于AA-BMP是两种耗竭方法中唯一均受影响的脂质物种,研究进一步探究了其在AD中的变化及与小胶质细胞的关联。在人类AD死后脑组织中,研究检测到异常的BMP积累,与5xFAD小鼠模型的趋势高度一致——含花生四烯酸(20:4)和油酸(18:1)的BMP物种显著升高,而含二十二碳六烯酸(DHA,22:6)的BMP物种则无明显变化,这一结果证实了BMP异常积累在AD中的临床相关性,也说明小鼠模型能很好地模拟人类AD的脂质病理特征。在小鼠模型中,尽管小胶质细胞干预并未使总体 BMP 水平发生显著改变,但不同类型的 BMP 分子对小胶质细胞耗竭呈现出截然不同的变化特征。其中,搭载花生四烯酸的 BMP 亚型对小胶质细胞耗竭高度敏感,在长期药理学干预后出现明显下降;在遗传学小胶质细胞敲除模型中,这两种 BMP 亚型同样表现出显著降低或相似的下调趋势。与之形成鲜明对比的是,含 DHA 的 BMP 亚型仅随淀粉样病理进程发生累积,其水平并不会因小胶质细胞的清除而下降,其中完全由 DHA 构成的 BMP 亚型在药理学处理组中保持稳定,在遗传学敲除组中甚至出现上升。这一结果充分说明,小胶质细胞仅特异性调控与 AD 病理密切相关的特定 BMP 亚型,而非整体 BMP 水平。
进一步分析发现,淀粉样变性会诱导溶酶体相关基因的异常上调,而两种小胶质细胞耗竭方法均能将这些基因的表达恢复至接近正常小鼠的水平。小胶质细胞 / 巨噬细胞特异性溶酶体标志物 CD68 的蛋白水平,同样在 5xFAD 小鼠脑中显著升高,而在长期药理学耗竭小胶质细胞后明显下降。作为溶酶体功能的另一重要指标,淀粉样病变诱导产生的异常高糖基化 LAMP1,在小胶质细胞耗竭后得到明显改善,正常分子量的LAMP1 则未受影响,说明清除小胶质细胞能够部分缓解 AD 中的溶酶体功能损伤。BMP 作为定位于晚期内体与溶酶体系统的特征性脂质,其水平可直接反映溶酶体功能状态,进一步分析显示,含花生四烯酸的 BMP 与溶酶体相关基因的表达水平呈现高度正相关,从分子层面印证了小胶质细胞通过调控溶酶体功能影响特定 BMP 代谢的核心机制。
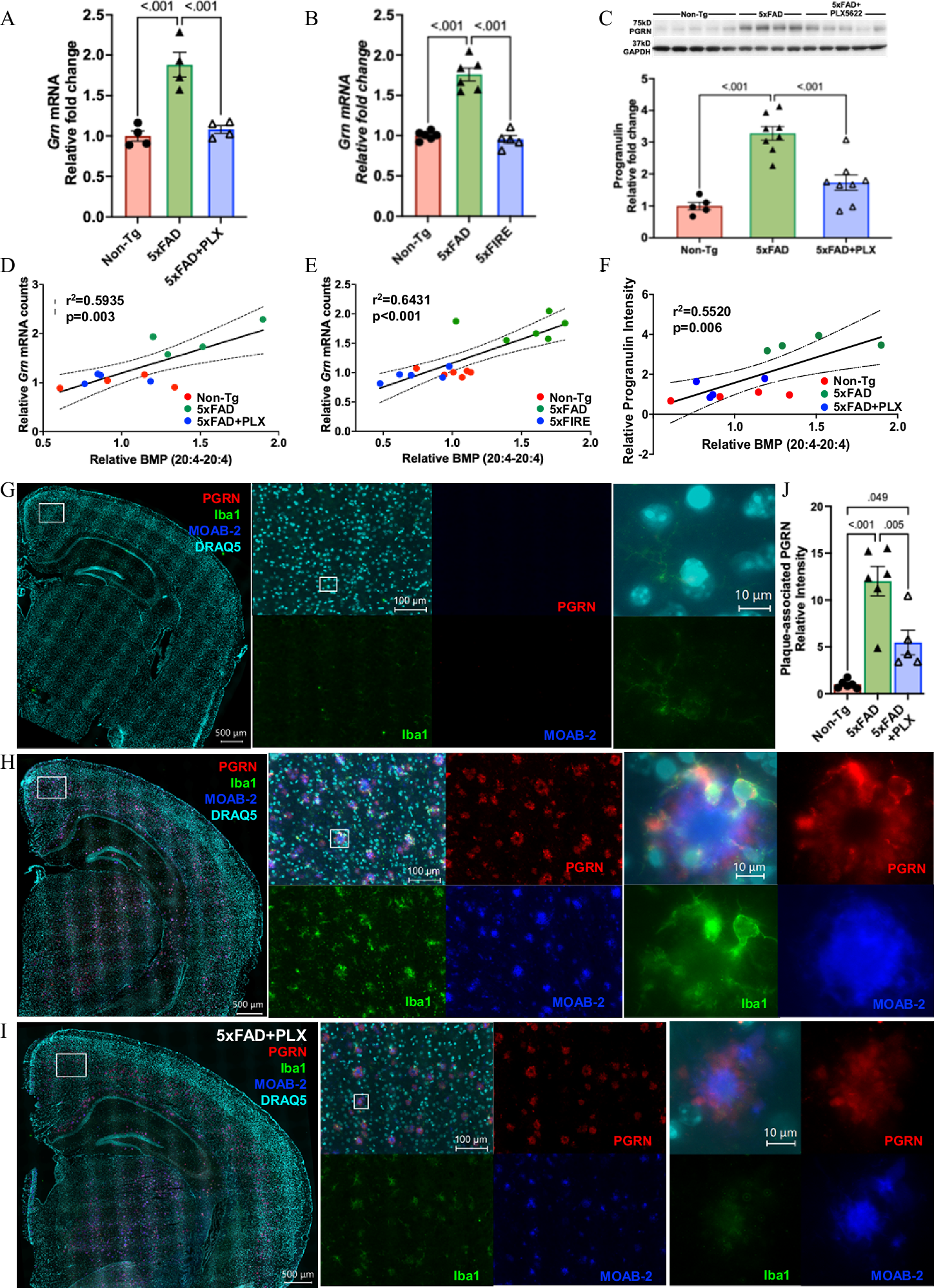
4、PGRN可能是AA-BMP的潜在调控因子
基于转录组分析和已有研究基础,研究聚焦于与溶酶体功能密切相关的颗粒体蛋白(PGRN),该蛋白与额颞叶痴呆、肌萎缩侧索硬化等神经退行性疾病相关,且临床研究已证实其与AD存在关联。实验发现,GRN在 5xFAD 模型小鼠中的表达水平显著高于正常对照小鼠,而长期药理学与遗传学小胶质细胞耗竭处理,均能有效抑制淀粉样病变所引起的GRN表达上调。在蛋白水平上,小胶质细胞的长期药理学耗竭,也可显著缓解淀粉样病变诱导的 PGRN 蛋白异常累积。
免疫荧光结果显示,PGRN在大脑中主要表达于小胶质细胞和神经元,且在围绕淀粉样斑块的反应性DAM中表达量最高,与Iba1、CD68等小胶质细胞标志物共定位,即使在PLX5622处理后,剩余的围绕斑块的DAM中仍有较高的PGRN表达,而小胶质细胞耗竭会显著减少斑块相关的PGRN积累,这与斑块负荷的降低和周围小胶质细胞的减少密切相关。相关性分析进一步证实,PGRN的mRNA和蛋白水平与AA-BMP水平高度相关,结合此前研究中GRN敲除小鼠大脑中BMP缺失的结论,明确了小胶质细胞来源的PGRN是AA-BMP代谢的潜在调控因子,揭示了小胶质细胞调控AA-BMP的具体分子机制,也将GRN基因与AD脂质代谢紊乱紧密关联起来。
5、小胶质细胞不驱动淀粉样变性诱导的溶血磷脂积累
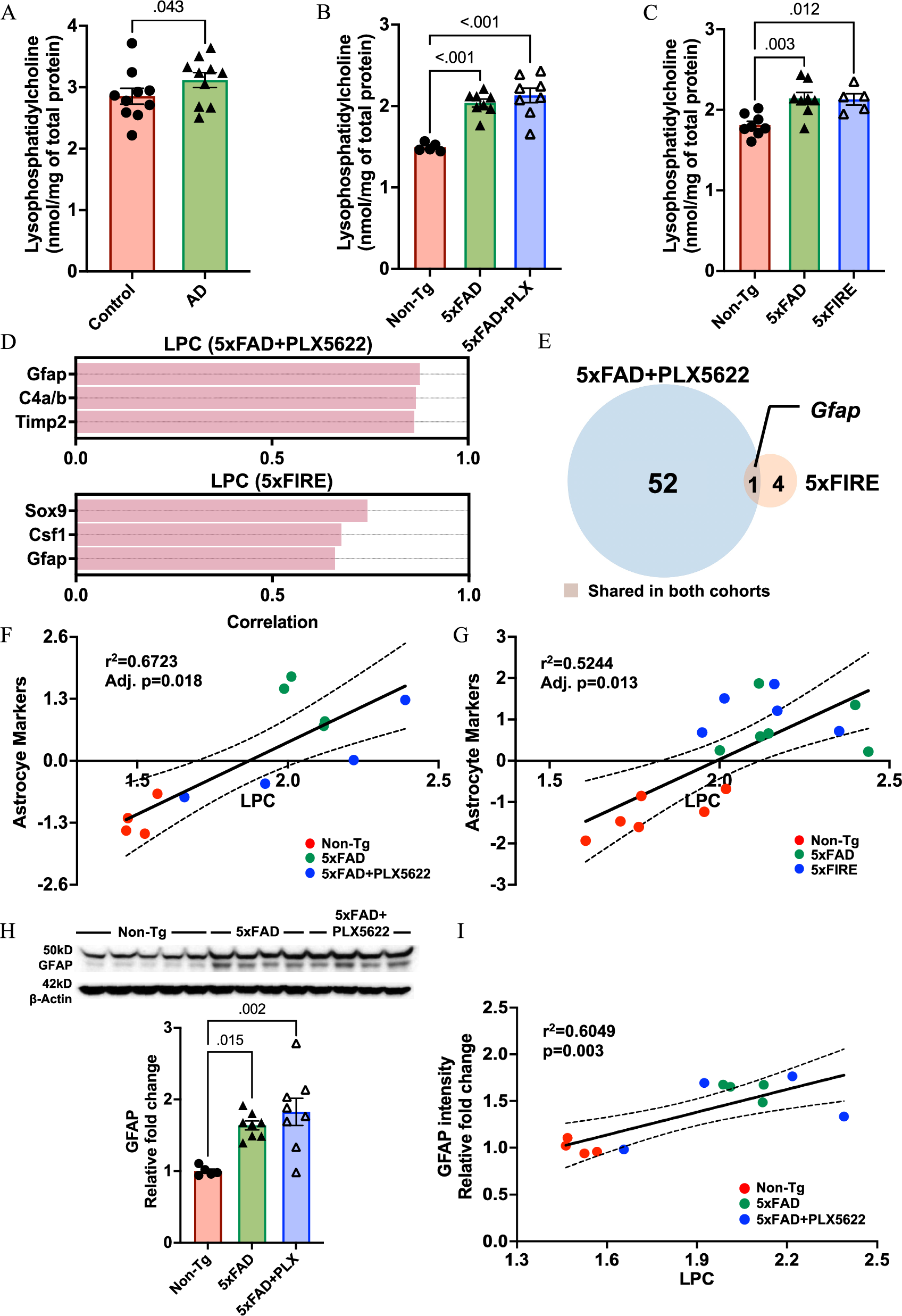
除BMP外,溶血磷脂酰胆碱(LPC)和溶血磷脂酰乙醇胺(LPE)作为AD的潜在生物标志物,其积累机制尚未明确。LPC 主要由磷脂酶 A2 水解细胞膜核心成分磷脂酰胆碱生成,不同亚型的 LPC 功能截然不同。饱和与单不饱和型 LPC 具备典型促炎作用,可推动趋化因子释放与活性氧生成,加剧神经炎症;而多不饱和型 LPC 则具有抗炎效果,能够抵消促炎亚型带来的损伤。本研究证实,总 LPC 水平在人类 AD 脑组织与淀粉样病变小鼠模型中均显著升高,且由多种亚型共同上调驱动。更关键的是,在淀粉样病变环境下,无论采用长期药理学处理还是遗传学敲除方式耗竭小胶质细胞,都无法改变总 LPC 含量,仅遗传学敲除会轻微降低多不饱和抗炎型 LPC,提示抗炎调控能力有所减弱。这一结果明确说明,淀粉样病变所诱导的促炎型 LPC 累积,完全不依赖小胶质细胞的参与。
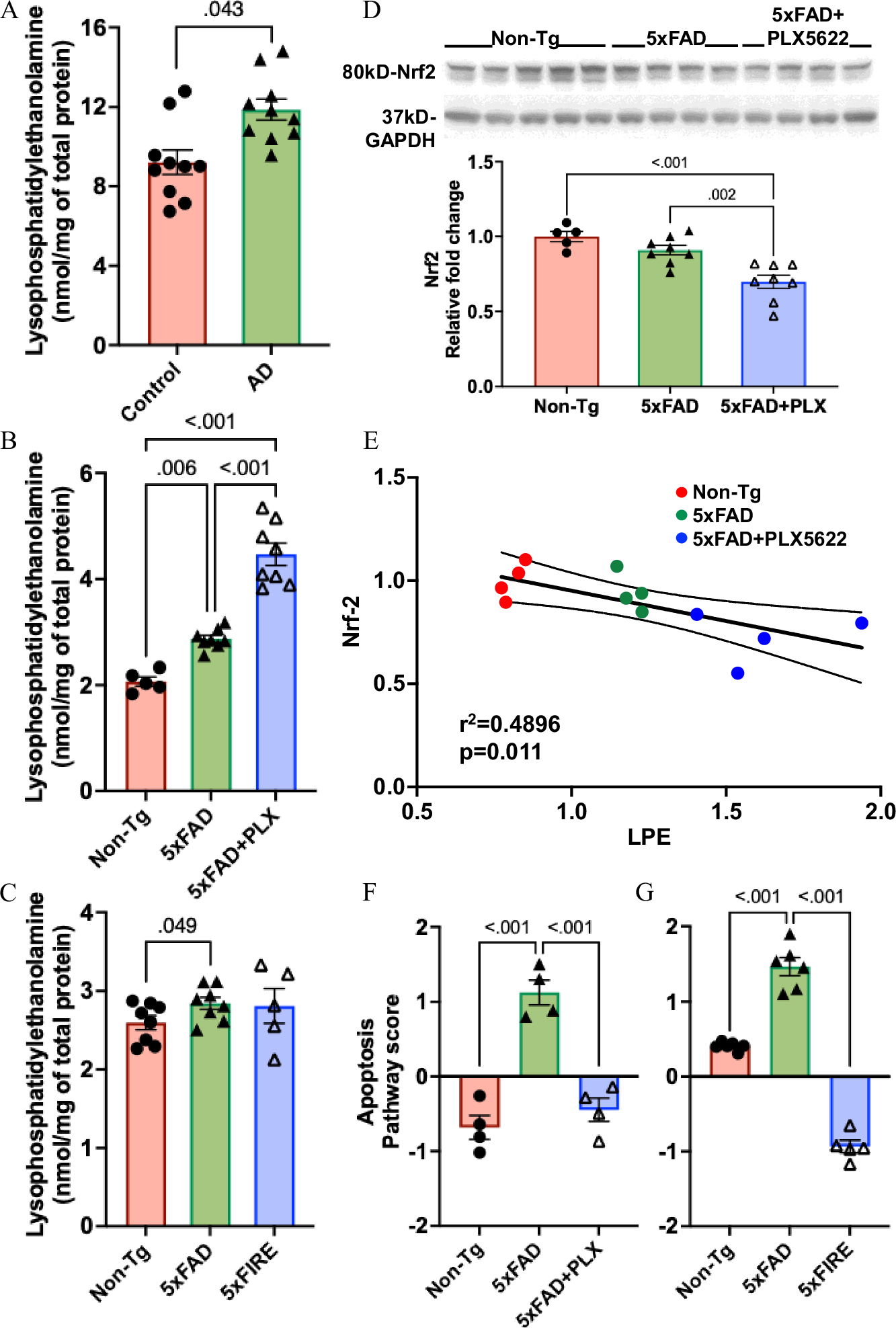
作为另一类关键溶血磷脂,LPE 由细胞膜及细胞器膜重要组分磷脂酰乙醇胺水解产生,它参与钙信号调控、具有抗凋亡活性,还能促进神经元分化与迁移,但其异常累积与氧化应激高度相关。研究发现,LPE 在 AD 患者脑组织和淀粉样病变小鼠模型中同样一致性升高,且呈现出明显的亚型特异性变化。意外的是,在淀粉样病变背景下,使用 PLX5622 长期部分清除小胶质细胞,会进一步加剧 LPE 的累积,其中非缩醛磷脂型 LPE 升高最为突出,这类物质可在活性氧攻击下由缩醛磷脂降解而来。虽然本研究未直接检测到氧化应激推动 LPE 累积的明确证据,但发现小胶质细胞耗竭后,核心抗氧化调控因子 Nrf2 表达下降,且与 LPE 水平呈负相关,提示小胶质细胞清除会削弱机体抗氧化应答,进而间接促进 LPE 异常上升。与药理学处理不同,遗传学小胶质细胞耗竭并未进一步升高 LPE。同时,在无淀粉样病变的情况下,完全清除小胶质细胞同样会导致 LPC 和 LPE 异常堆积,而短期小胶质细胞耗竭则无明显影响,这与早期病理程度较轻有关。
综合以上结果可以确定,在阿尔茨海默病进程中,LPC 与 LPE 的异常累积并非由小胶质细胞主导驱动,LPC 主要与星形胶质细胞活化相关,而 LPE 更多受氧化应激调控,这一发现为理解 AD 脂质紊乱的细胞特异性机制提供了重要依据。
四、总结
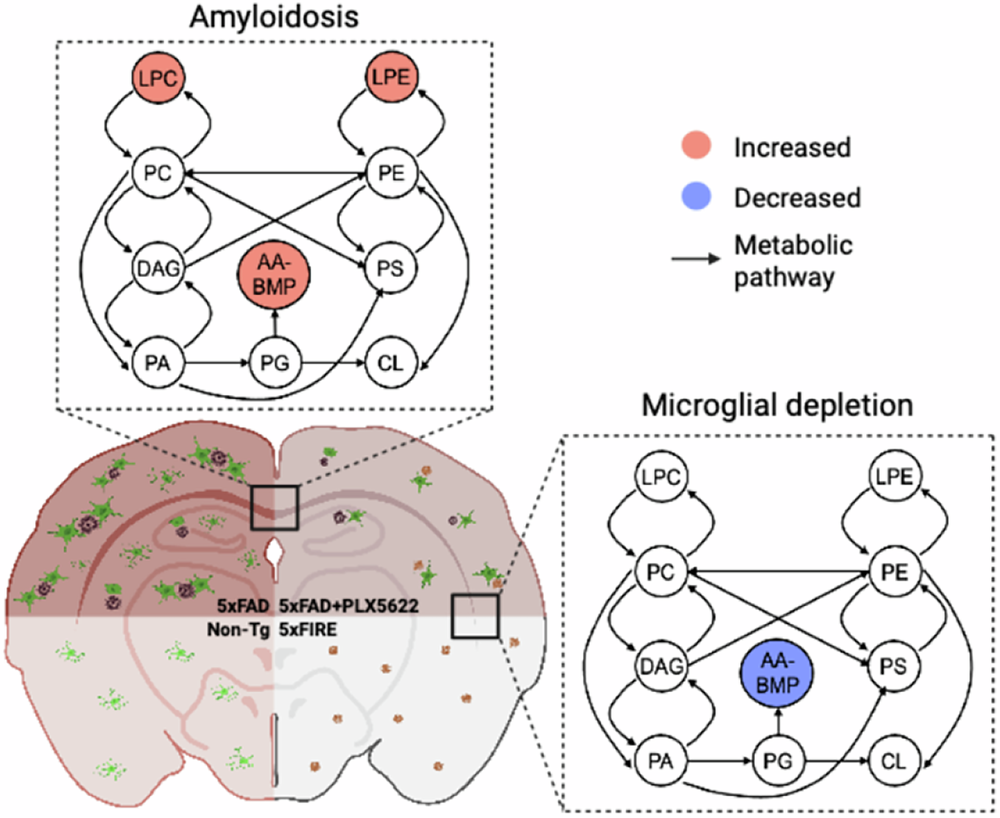
该研究通过严谨的实验设计,结合小鼠模型与人类样本,首次系统揭示了小胶质细胞对AD脂质代谢的特异性调控作用,明确了不同脂质物种的调控机制与细胞来源,小胶质细胞通过PGRN调控溶酶体功能,进而特异性控制AA-BMP的积累,且这种调控独立于淀粉样变性;而LPC和LPE的积累则依赖于星形胶质细胞激活和氧化应激,与小胶质细胞无关。研究不仅将AD中的脂质代谢紊乱与特定脑细胞类型、分子通路相关联,破解了长期以来AD脂质代谢调控机制的困惑,还将 Alois Alzheimer 最初观察到的脂质聚集与基因定义的脂质通路联系起来,为AD治疗提供了新的靶点——小胶质细胞脂质稳态,尤其针对AA-BMP和PGRN的调控,有望成为改善AD病理进展的潜在策略。同时,该研究也为后续AD脂质代谢研究提供了新的思路,即从细胞特异性角度解析脂质紊乱的机制,为精准治疗奠定基础。
参考文献
Xu Z, Kiani Shabestari S, Barannikov S, Bieniek KF, Blurton-Jones M, Palavicini JP, Han X. Microglia-specific regulation of lipid metabolism in Alzheimer's disease revealed by microglial depletion in 5xFAD Mice. Nat Commun. 2025 Oct 15;16(1):9156. doi: 10.1038/s41467-025-64161-z. PMID: 41093842; PMCID: PMC12528747.
EnkiLife恩玑生命产品:
