THP-1细胞培养的注意事项,以及实验的应用场景
THP-1细胞是从一名罹患急性单核细胞性白血病的1岁男孩的外周血中分离建系。THP-1细胞对乳胶微粒和致敏红细胞有吞噬作用,细胞膜和胞浆内均没有免疫球蛋白,该细胞表达C3R和FcR。THP-1细胞在含PMA(50-100 nM)的培养条件下分化为巨噬细胞,而在GM-CSF联合IL-4(各100 ng/mL)的细胞因子组合下则分化为树突状细胞。THP-1可用于与其他类型的细胞(如肿瘤细胞)共培养,以更好地模拟体内条件,用于免疫应答研究。作为目前最成熟的单核细胞系,THP-1已广泛应用于免疫学、癌症和药物毒理学研究。

THP-1细胞培养注意事项
- 该细胞属于悬浮细胞,传代时建议采用半换液法,更有利于维持细胞良好状态。请勿通过离心收集细胞,可直接向培养瓶内加入等体积新鲜培养液,吹打均匀后分至两个新的T25培养瓶中继续培养(即1:2传代)。
- 培养过程中,个别细胞可能出现形态偏大的情况,也可能有少量细胞贴壁或聚集成小团生长,这些均属正常现象。传代时可轻轻打散细胞团;若有少量细胞已贴壁,传代时可直接丢弃;小团生长的细胞正常传代培养即可。
- 该细胞对密度较为敏感,培养及传代过程中需注意维持细胞密度在适宜范围(具体请参照细胞说明书)。
- 冻存该细胞时需提高细胞密度,建议当1个T25培养瓶内细胞量达到300-500万时冻存一支。
- 该细胞对血清质量敏感,建议使用优质胎牛血清进行培养。
THP-1细胞的应用
1. 炎症模型构建与抗炎药物筛选
脂多糖(Lipopolysaccharide, LPS)诱导的THP-1巨噬细胞炎症模型是研究人源巨噬细胞介导炎症反应的重要体外模型。与RAW264.7小鼠巨噬细胞系相比,THP-1作为人源细胞系,在模拟人体炎症微环境和药物反应方面具有不可替代的种属优势。
Guo Shuyun[1]等人借助体内LPS诱导的大鼠急性肺损伤模型与体外 LPS+ATP 诱导的THP-1巨噬细胞模型,探究了远志提取物(Polygala tenuifolia willd. Extract, EPT)的抗炎作用及潜在机制。在这项研究中,THP-1细胞被用作炎症反应的体外研究模型,研究人员先通过PMA诱导THP-1细胞贴壁分化为巨噬细胞样细胞,再经LPS联合ATP处理激活细胞炎症表型,模拟急性肺损伤过程中巨噬细胞的过度活化状态,随后将不同浓度的远志含药血清与激活的THP-1细胞共培养。远志含药血清处理后,研究人员通过qPCR与蛋白免疫印迹实验检测发现,THP-1细胞的炎症状态发生显著改善:促炎因子TNF-α、IL-1β、IL-6、iNOS的基因表达水平显著下调,且TLR4/NF-κB信号通路相关蛋白TLR4、MyD88、p-IκBα、p-p65,以及NLRP3炎症小体相关蛋白NLRP3、ASC、cleaved caspase-1、cleaved IL-1β的表达均呈明显下调趋势(如图2,图3,图4)。这一结果揭示,远志提取物通过抑制TLR4/NF-κB信号通路与NLRP3炎症小体的激活,减少促炎因子的释放与成熟,有效阻断了LPS+ATP诱导的炎症级联反应,表明其具有显著的体外抗炎活性,为其作为治疗急性肺损伤的潜在药物提供了实验依据。
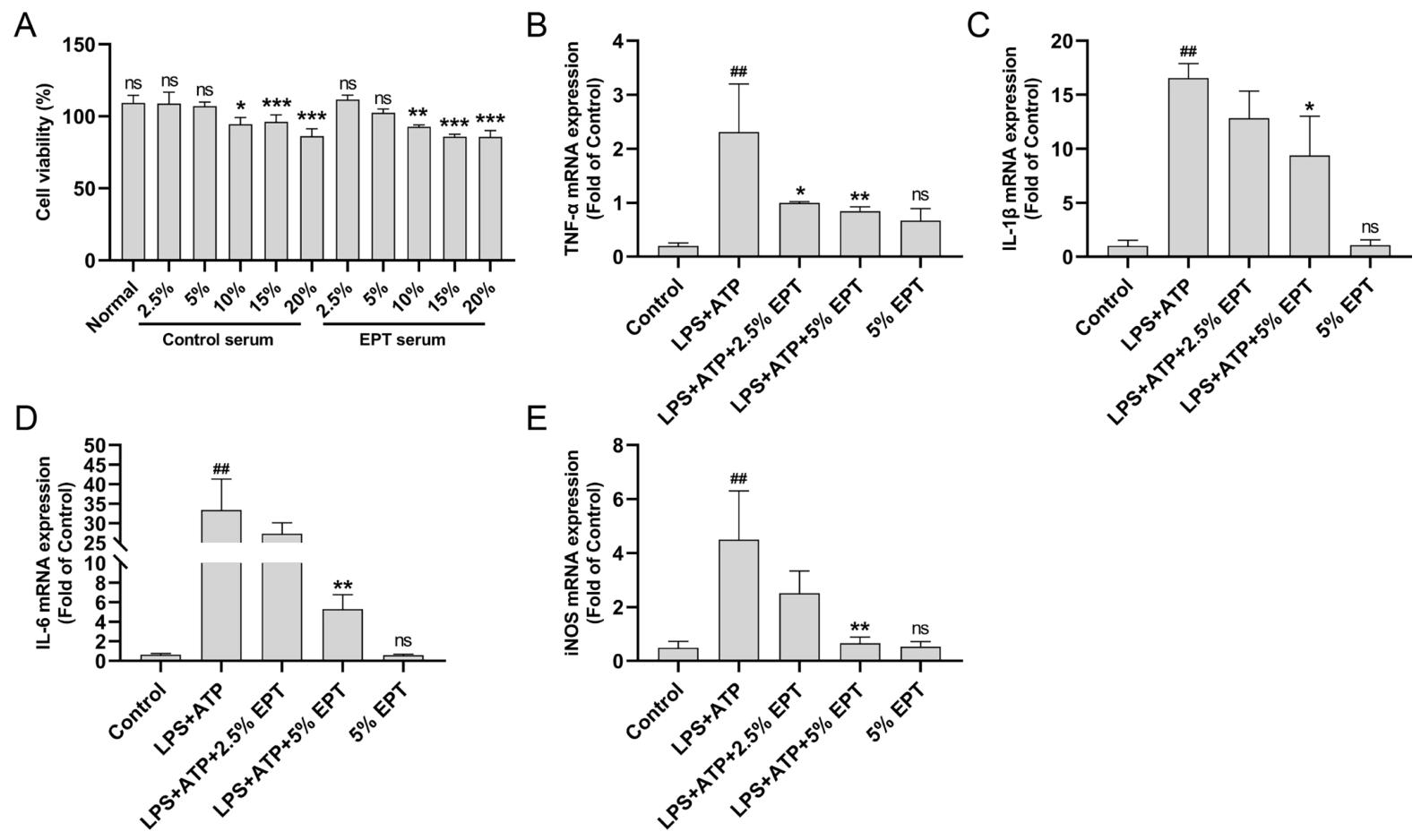
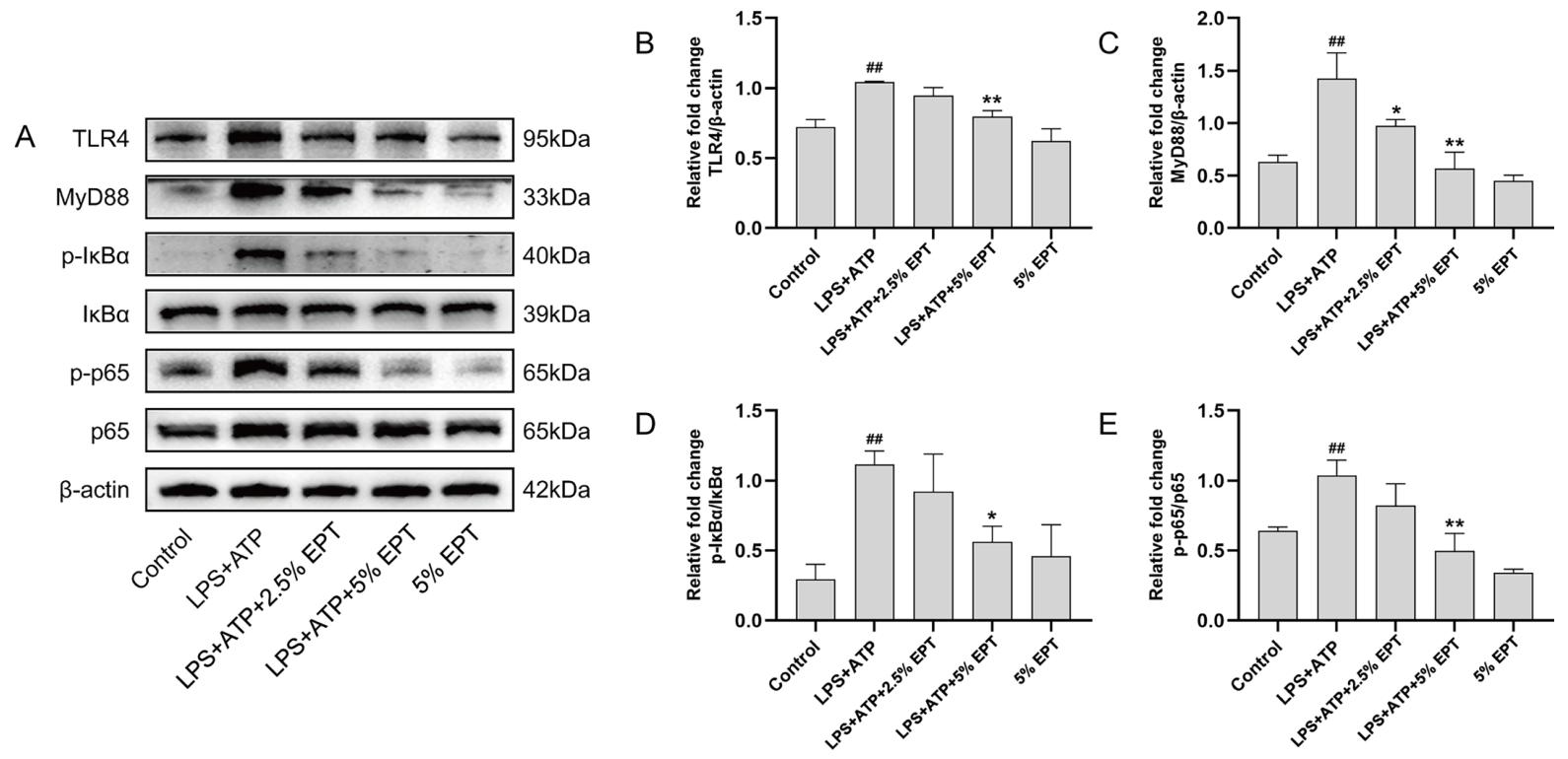
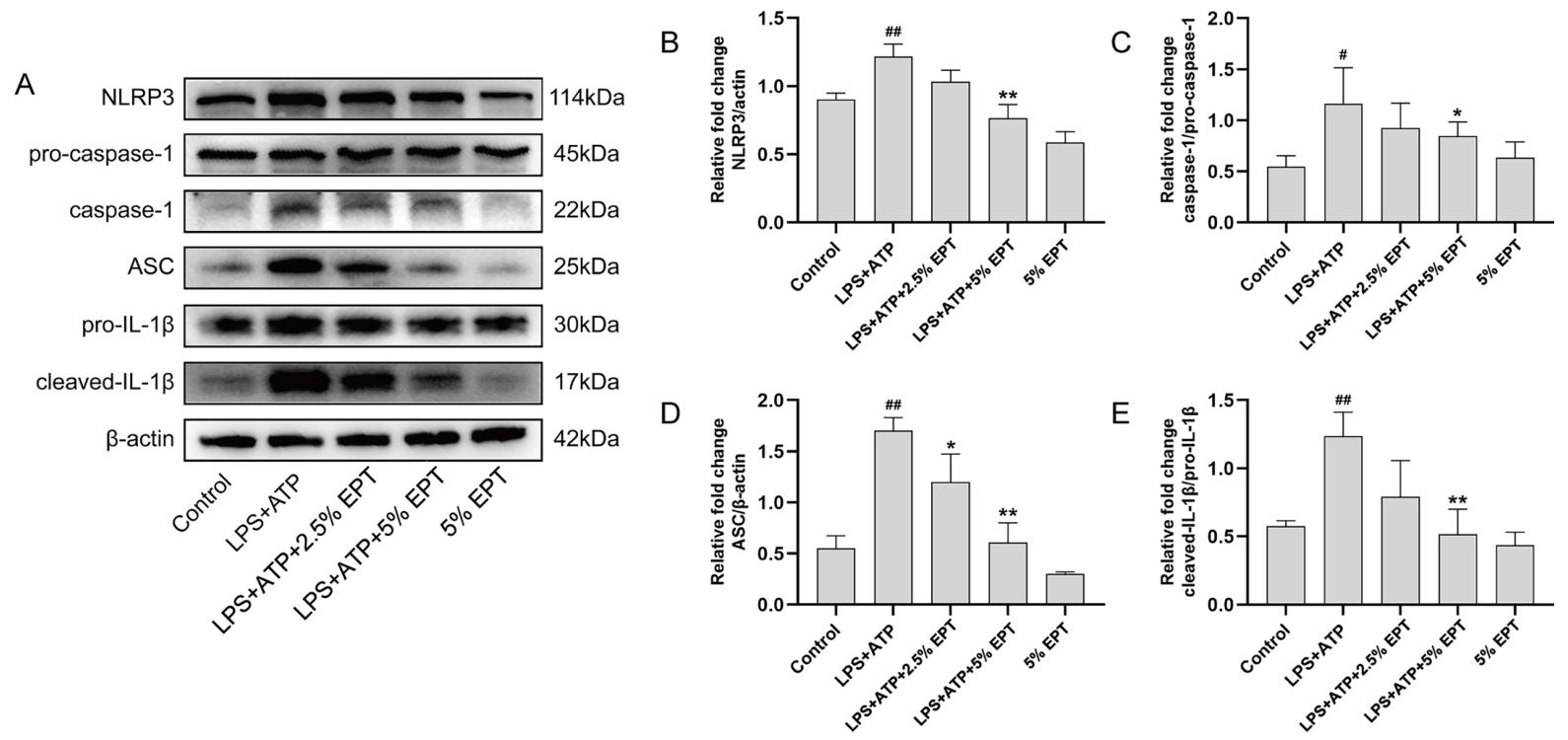
2. 免疫调节研究
THP-1细胞可模拟人体单核细胞向巨噬细胞的分化过程,用于研究先天免疫细胞如何识别病原体、启动免疫反应,以及相关信号通路(如NF-κB、JAK-STAT等)的激活机制。通过诱导THP-1细胞分化为M1(促炎型)或M2(抗炎型)巨噬细胞,研究巨噬细胞在免疫调节、炎症反应、组织修复等过程中的功能差异和调控机制。
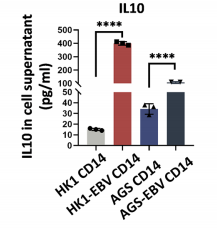
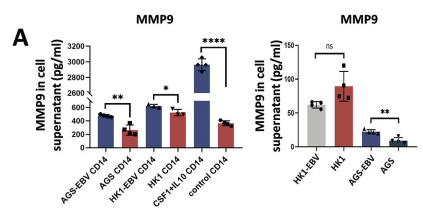
Chen Yuanyuan[2]等人借助体内EBV阳性肿瘤小鼠异种移植模型与体外 EBV感染肿瘤上清诱导的THP-1巨噬细胞模型,探究了EBV调控巨噬细胞极化及介导TCR-T细胞疗法抵抗的分子机制与干预策略。在这项研究中,THP-1细胞被用作巨噬细胞极化的体外研究模型,研究人员先利用EBV感染或未感染的肿瘤细胞上清处理THP-1细胞,模拟EBV阳性肿瘤微环境对巨噬细胞的极化诱导状态,再通过流式细胞术检测巨噬细胞表面标志物的表达特征,同时设置CSF1、IL10单独及联合处理组作为对照。经EBV感染肿瘤上清处理后,研究人员通过流式细胞术与ELISA实验检测发现,THP-1细胞的极化表型发生显著改变:M2型巨噬细胞特异性标志物CD163的表达水平显著上调,且巨噬细胞的IL10自分泌能力与MMP9的分泌水平均呈明显升高趋势(如图5,图6,图7)。这一结果揭示,EBV可通过肿瘤上清介导的CSF1与IL10协同作用,诱导THP-1细胞向CD163+M2型巨噬细胞极化,且该极化后的巨噬细胞会大量分泌MMP9,为阐释EBV阳性肿瘤微环境中M2巨噬细胞介导T细胞耗竭与TCR-T疗法抵抗的机制提供了重要的细胞模型实验依据,也为后续靶向M2巨噬细胞及MMP9的干预研究奠定了体外基础。
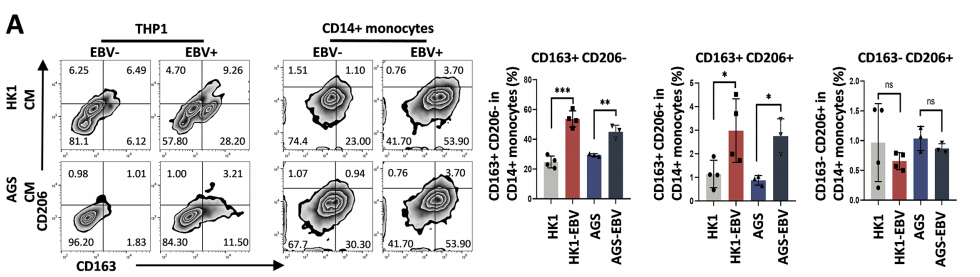
3. 心血管疾病研究
THP-1细胞通过PMA诱导成巨噬细胞后,加入50μg/mL氧化型低密度脂蛋白(ox-LDL)孵育48小时,诱导为泡沫细胞,泡沫细胞的形成是动脉粥样硬化形成的早期事件,是动脉粥样化斑块内出现的特征性病理细胞。
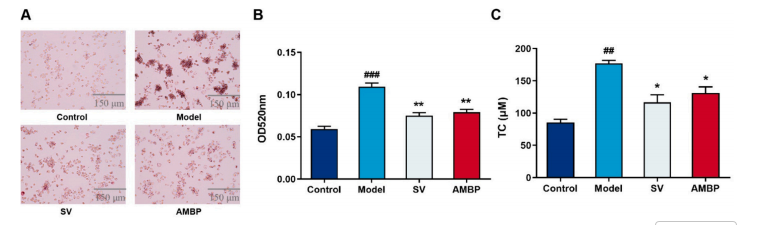
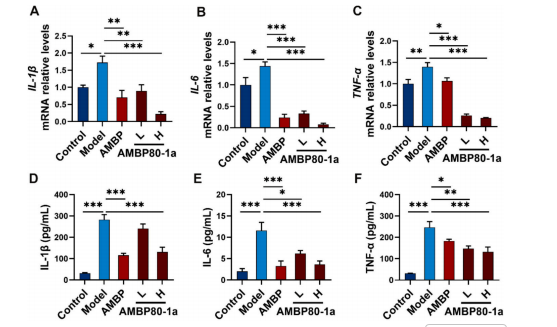
Pei Lin[3]等人利用体内高脂饮食诱导的动脉粥样硬化ApoE⁻/⁻小鼠模型和体外ox-LDL诱导的THP-1巨噬细胞,研究了大葱多糖(AMBP及其纯化组分AMBP80-1a)的抗动脉粥样硬化潜力。在这项研究中,THP-1细胞被用作动脉粥样硬化的体外模型。研究人员首先使用佛波酯(PMA)诱导THP-1单核细胞分化为巨噬细胞,再经氧化低密度脂蛋白(ox-LDL)处理,诱导其形成泡沫细胞,模拟动脉粥样硬化状态下巨噬细胞的脂质蓄积与炎症激活反应。随后,将大葱粗多糖AMBP及纯化的均一多糖AMBP80-1a分别与激活的THP-1巨噬细胞共培养。处理后,研究人员通过生化检测与染色分析发现,THP-1泡沫细胞的病理状态发生显著改善:细胞内脂质滴数量明显减少,总胆固醇(TC)含量显著降低,且促炎因子肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)和白细胞介素-1β(IL-1β)的mRNA表达及蛋白分泌水平均显著下调(如图7,图8)。RT-qPCR结果进一步揭示,AMBP及AMBP80-1a通过调控炎症反应、胆固醇摄取与流出相关基因的表达,有效阻断了ox-LDL诱导的泡沫细胞形成与炎症级联反应。这表明大葱多糖尤其是AMBP80-1a具有显著的体外抗动脉粥样硬化活性,为其作为预防和治疗动脉粥样硬化的潜在功能因子提供了实验依据。
实验方案
THP-1诱导分化成M0型巨噬细胞实验步骤:
(1) THP-1细胞的培养
(2) 诱导培养基的配置:向1640完全培养基(含胎牛血清)里加入PMA(诱导浓度:100ng/mL[4])制成诱导培养基;
(3) 接种细胞:收集THP-1细胞并进行计数,用诱导培养基重悬细胞沉淀调整细胞密度为5×105/mL,将细胞种入六孔板,每孔加入细胞悬液2mL;
(4) 诱导培养:培养24h后用新鲜培养基静置24小时;
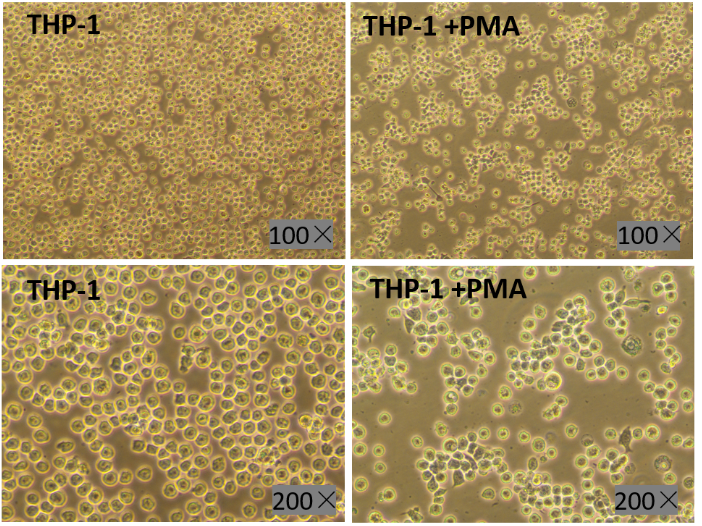
诱导成功的标志:单核细胞THP-1用PMA诱导后,由悬浮式生长变成贴壁生长,由圆形变成不规则形态,体积进一步增大,细胞浆疏松,细胞核增大明显,可见大量明显细胞器,胞膜周围可见少量突起(如图9)。
巨噬细胞进一步诱导成M1型实验步骤:
(1) 诱导培养基的配制:向含胎牛血清的1640完全培养基中加入脂多糖(LPS,诱导浓度100ng/mL[4])与IFN-γ(诱导浓度20ng/mL[4]),配制得到诱导培养基;
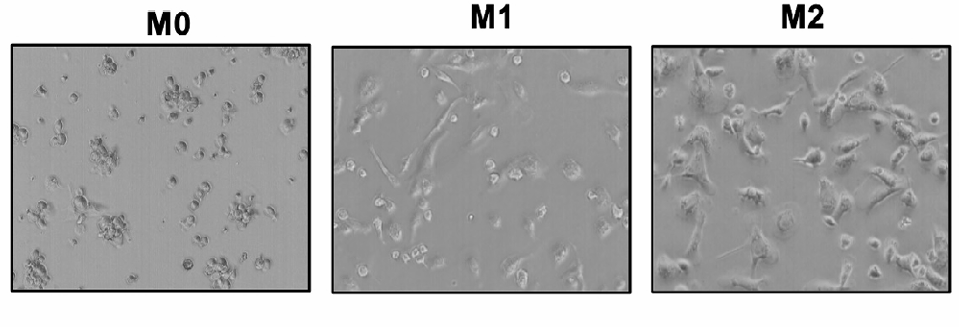
(2) 诱导培养:弃去已诱导形成的M0型巨噬细胞的培养基,加入诱导培养基(6孔板,每孔2mL)培养24小时,诱导其向M1型极化;培养24小时后,通过显微镜观察验证M1型细胞是否构建成功;
(3) 最后,在无刺激物及无PMA的条件下,使用无血清RPMI-1640基础培养基重悬细胞,该状态可维持72小时。
巨噬细胞进一步诱导成M2型实验步骤:
(1) 诱导培养基的制备:向含胎牛血清的1640完全培养基中加入IL-4(诱导浓度20ng/mL[4])与IL-13(诱导浓度20ng/mL[4]),即得诱导培养基;
(2) 诱导培养:弃去已诱导获得的M0型巨噬细胞的培养基,加入诱导培养基(6孔板每孔2mL)培养24h,诱导其向M2型极化。24h后,通过显微镜观察M2型细胞是否诱导成功;
(3) 最后,在无刺激物及PMA的条件下,使用无血清RPMI-1640基础培养基重悬细胞,可使细胞维持72h。
诱导泡沫化
(1) 诱导培养基的制备:向1640基础培养基中加入ox-LDL(诱导浓度为50μg/mL[8]),配制得到诱导培养基;
(2) 诱导培养:将已诱导形成的M0型巨噬细胞的培养基弃去,加入诱导培养基(6孔板,每孔2mL)孵育48h,使其转化为泡沫细胞;
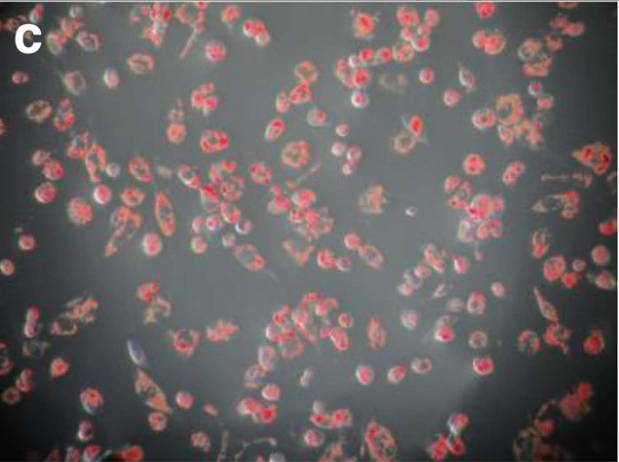
(3) 诱导完成后,通过倒置显微镜观察发现,巨噬细胞体积进一步增大,细胞膜突触形成显著,胞浆增多且疏松化,可见大量细胞器及吞噬的脂质小滴;经油红O染色后,胞浆内可见大量红染物质。
参考文献:
- Guo S, Zhang J, Zhang Q, et al. Polygala tenuifolia willd. Extract alleviates LPS-induced acute lung injury in rats via TLR4/NF-κB pathway and NLRP3 inflammasome suppression. Phytomedicine. 2024;132:155859.
- Chen Y, Ouyang D, Wang Y, et al. EBV promotes TCR-T-cell therapy resistance by inducing CD163+M2 macrophage polarization and MMP9 secretion. J Immunother Cancer. 2024;12(6):e008375. Published 2024 Jun 17.
- Lin P, Wang Q, Wang Q, et al. Evaluation of the anti-atherosclerotic effect for Allium macrostemon Bge. Polysaccharides and structural characterization of its a newly active fructan. Carbohydr Polym. 2024;340:122289.
- Horiba S, Kami R, Tsutsui T, Hosoi J. IL-34 Downregulation‒Associated M1/M2 Macrophage Imbalance Is Related to Inflammaging in Sun-Exposed Human Skin. JID Innov. 2022;2(3):100112. Published 2022 Feb 24.
- Liu T, Huang T, Li J, et al. Optimization of differentiation and transcriptomic profile of THP-1 cells into macrophage by PMA. PLoS One. 2023;18(7):e0286056. Published 2023 Jul 17.
- Mazan A, Marusiak AA. Protocols for Co-Culture Phenotypic Assays with Breast Cancer Cells and THP-1-Derived Macrophages. J Mammary Gland Biol Neoplasia. 2024;29(1):4. Published 2024 Feb 10.
- Song Z, Xia H, Yang L, Wang S, Sun G. Lowering the n-6/n-3 PUFAs ratio inhibits the formation of THP-1 macrophage-derived foam cell. Lipids Health Dis. 2018;17(1):125. Published 2018 May 25.
- Lin P, Wang Q, Wang Q, et al. Evaluation of the anti-atherosclerotic effect for Allium macrostemon Bge. Polysaccharides and structural characterization of its a newly active fructan. Carbohydr Polym. 2024;340:122289.
注:本文档中图片均源自原文献附图示意,因原始文档提供图片路径引用,展示为占位说明,所有学术内容及文字描述均严格保留原文。
 | Flora Flora是EnkiLife的技术支持专家,熟悉免疫学和神经科学,致力于为客户提供高品质的产品搭配和技术支持,以帮助实现神经退行性疾病和其它神经科学方面的研究。 |
