文献解析|TRPM4 的持续激活触发以钠超载为特征的坏死性细胞死亡

这篇发表于《Nature Chemical Biology》的研究是细胞死亡领域的重要突破,首次鉴定出以钠超载为核心特征的新型程序性坏死方式 ——NECSO(Necrosis by Sodium Overload),明确了瞬时受体电位阳离子通道 TRPM4 是该过程的核心调控分子,并解析了其分子机制、物种特异性及疾病关联,同时筛选出首个 NECSO 抑制剂,为细胞死亡调控和相关疾病治疗提供了全新靶点与策略。
一、研究背景
过量的钠离子与多种人类疾病(如高血压、心血管疾病、脑水肿等)密切相关。虽然钙、铁、铜等离子的超载已被证实可直接导致细胞死亡,但钠离子超载是否具有类似的直接致病机制尚不清楚。该研究鉴定了一种名为“Necrocide 1”(NC1)的手性小分子化合物,它能诱导一种独特的免疫原性坏死性细胞死亡,且不被已知的凋亡、坏死性凋亡、自噬或铁死亡抑制剂所阻断。
研究团队通过全基因组CRISPR-Cas9筛选,发现瞬时受体电位阳离子通道亚家族M成员4(TRPM4)是NC1的关键靶点。NC1通过特异性地激活人源TRPM4(hTRPM4),导致大量钠离子内流,进而引发细胞坏死。这种新型细胞死亡方式被命名为“钠超载诱导的坏死”(NECSO)。
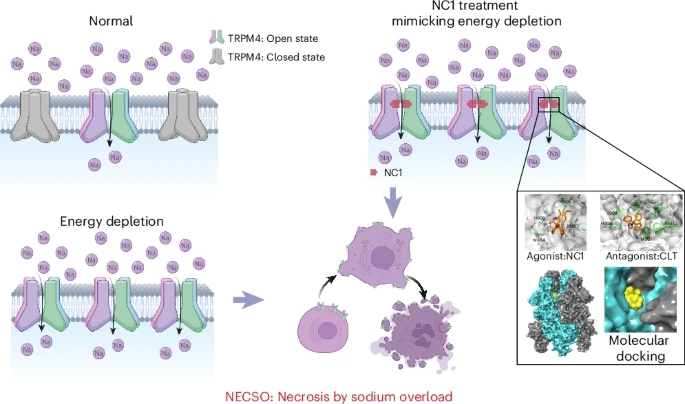
二、研究结果
1. TRPM4是NC1诱导细胞死亡的关键因子
研究通过全基因组CRISPR-Cas9筛选发现TRPM4基因是NC1抵抗性细胞中富集度最高的候选基因。在MCF7细胞中敲除TRPM4可完全阻断NC1诱导的细胞死亡和乳酸脱氢酶(LDH)释放,而重新表达人源TRPM4则可恢复其对NC1的敏感性。此外,TRPM4的离子通道活性对于NC1诱导的坏死至关重要,因为重新表达离子不可渗透的突变体D984A无法挽救坏死表型。
实验证实NC1直接与TRPM4结合,细胞热位移实验(CETSA)显示NC1在高温下能稳定TRPM4蛋白,且表面等离子共振(SPR)分析测得亲和力为0.88 μM。全细胞膜片钳记录显示,NC1能诱导TRPM4依赖的电流,且这种激活具有持续性,即使在洗脱后电流也不会消失,这表明NC1导致TRPM4通道的持续和不可逆激活。
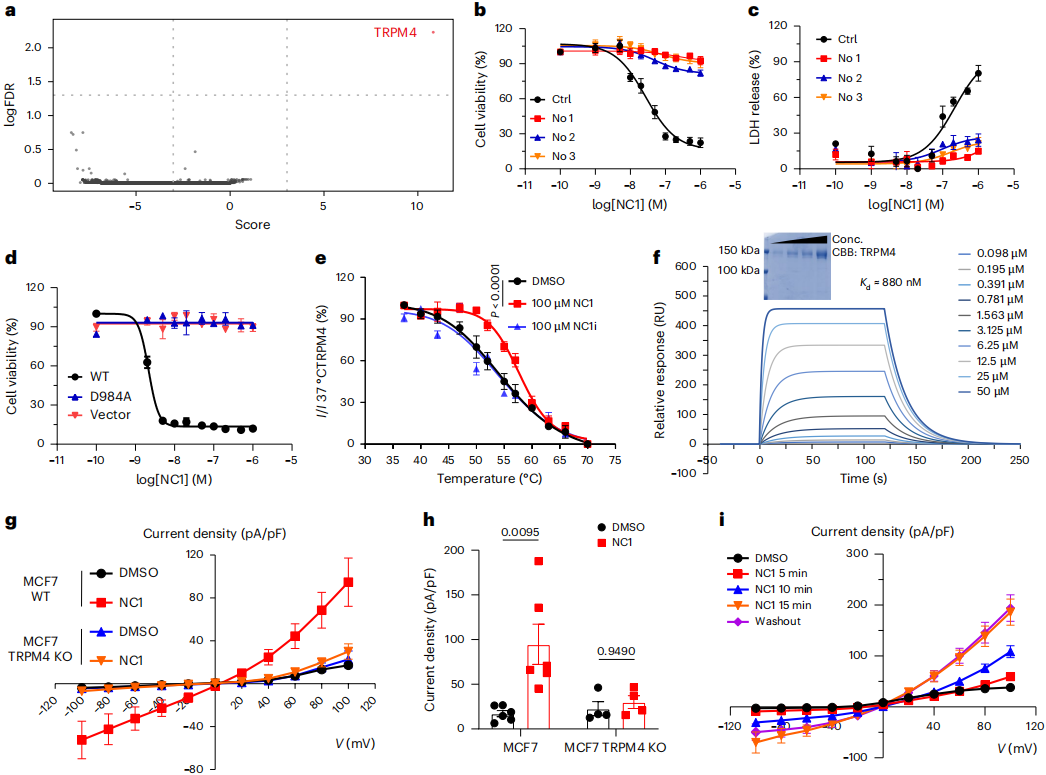
图1 | NC1触发依赖于TRPM4的独特细胞死亡途径。
2. NC1 通过 TRPM4 诱导的坏死依赖钠离子内流
TRPM4作为非选择性单价阳离子通道,其激活导致钠离子大量内流。电感耦合等离子体质谱(ICP-MS)分析显示NC1处理后细胞内钠水平显著升高。通过替换细胞外液中的钠离子,研究发现钠离子的耗竭能显著阻断细胞死亡,而抑制钾外流则无明显影响,证明了钠内流而非钾外流是导致细胞坏死的关键因素。这种由钠超载引起的细胞死亡被定义为“钠超载诱导的坏死”(NECSO)。
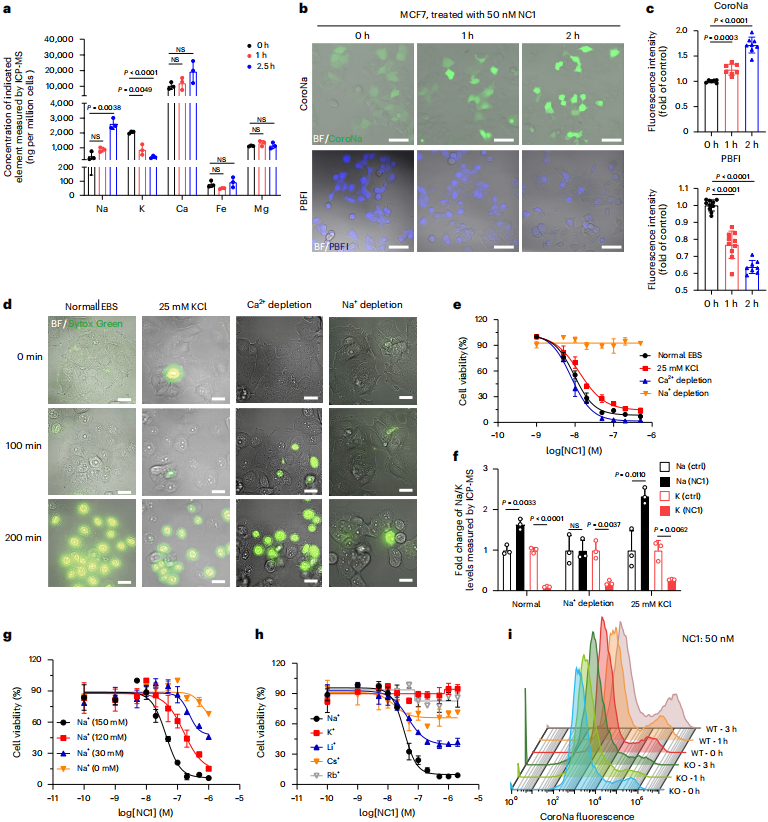
图2 | 钠离子内流是NC1诱导细胞死亡的关键。
3. NC1 特异性靶向人类 TRPM4
研究指出,NC1特异性激活人源TRPM4,而对小鼠源TRPM4(mTRPM4)无激活作用,尽管两者具有88.4%的序列相似性。通过构建人鼠嵌合体蛋白,研究人员确定跨膜区是决定NC1敏感性的关键区域。这些结果表明,NC1 是人类 TRPM4 的高特异性激动剂,仅能在表达 hTRPM4 的细胞中诱导钠过载性坏死。
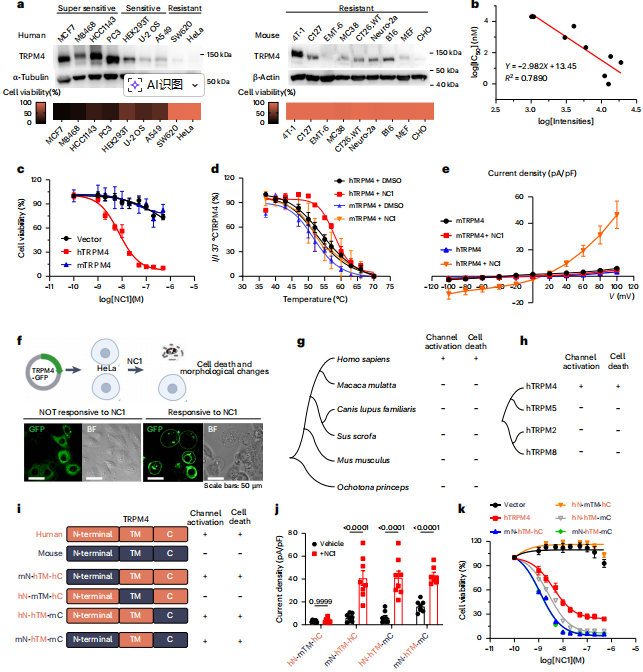
图 3 | NC1 通过与跨膜区的相互作用特异性靶向人类 TRPM4
4. 分子对接鉴定 NC1 激活 TRPM4 的关键氨基酸残基
分子对接和突变分析揭示,NC1结合在TRPM4跨膜区的一个类似香草素结合口袋(VBP),该位点涉及S3、S4、S5和S6螺旋上的关键残基。将关键残基(如W864, H908, F936)突变为丙氨酸会破坏NC1的结合和通道激活,证实了该结合口袋是 NC1 诱导 TRPM4 激活的必要结构。
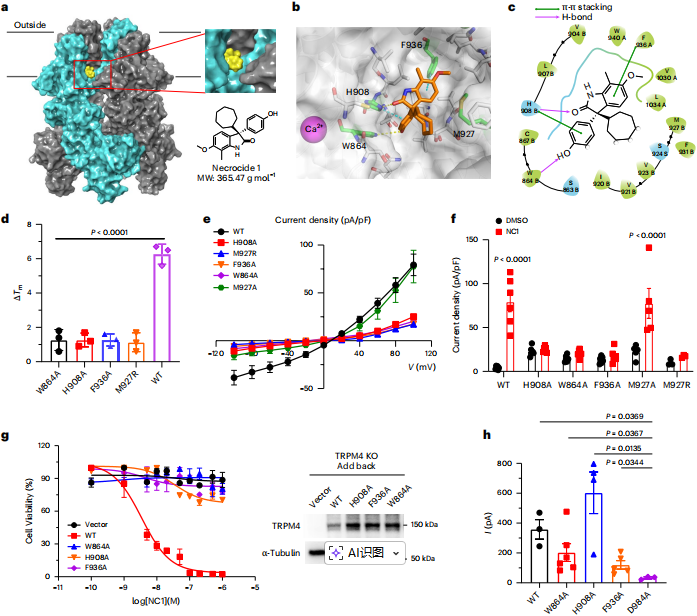
图4 | 通过分子对接和突变分析揭示了TRPM4中对于NC1激活至关重要的残基。
5. 能量耗竭诱导的坏死与钠过载性坏死具有共同特征
研究发现,能量耗竭(如2DG+NaN₃处理)也能激活TRPM4并引发钠内流和坏死,这与NC1诱导的NECSO具有相似的遗传和化学干预特征。此外,与心脏疾病相关的TRPM4功能获得性突变体对NC1或能量耗竭诱导的细胞死亡表现出更高的敏感性。
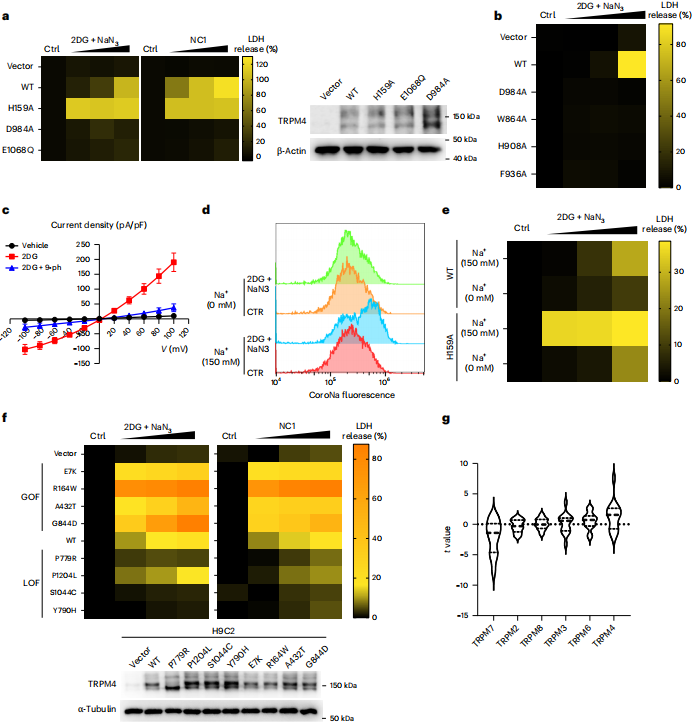
图 5 | 能量耗竭诱导的细胞死亡与钠过载性坏死具有共同特征
6. 发现NECSO的潜在抑制剂
研究鉴定了克霉唑(CLT)和二氢吡啶类化合物(DHPs)可作为NECSO的抑制剂。CLT通过直接竞争结合TRPM4抑制NECSO,而DHPs则作为L型电压门控钙通道阻滞剂间接抑制这一过程。这些抑制剂能有效保护心肌细胞免受TRPM4功能获得性突变相关的细胞损伤。
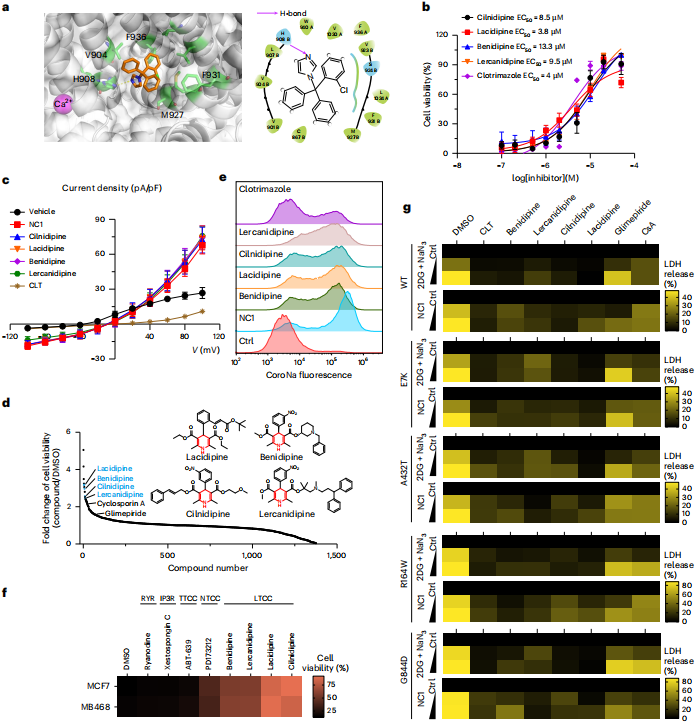
图6 | DHPs和CLT作为NECSO的小分子抑制剂发挥作用
三、总结
该研究不仅定义了一种由钠离子超载驱动的新型细胞坏死形式NECSO,还揭示了其核心执行蛋白TRPM4及其特异性激动剂NC1的作用机制。这一发现将细胞死亡研究与钠离子稳态联系起来,为理解缺血性损伤、心力衰竭及TRPM4相关疾病的病理机制提供了新视角。此外,CLT和DHPs作为潜在的治疗药物,展示了通过靶向TRPM4或其相关通路来干预细胞死亡的可行性。
文献来源
Fu W, et al. Persistent activation of TRPM4 triggers necrotic cell death characterized by sodium overload. Nat Chem Biol. 2025 Aug;21(8):1238-1249. doi: 10.1038/s41589-025-01841-3. Epub 2025 Feb 6. PMID: 39915626.
该研究所涉及的抗体,EnkiLife恩玑生命均可提供:
Catalog# | Product Name | Reactivity | Application |
APRab19320 | TRPM4 Rabbit Polyclonal Antibody | Human,Mouse,Rat | WB |
AMRe07987 | Caspase-9 (13Z10) Rabbit Monoclonal Antibody | Human,Mouse | WB,IHC-P,ICC/IF,FC,IP,IF-P |
AMM80017 | α-tubulin Monoclonal Antibody(8F11) | Human,Mouse,Rat | WB,IHC-P,IF-P,IF-F,IF-ICC,IP,Elisa |
APRab80018 | α-tubulin Polyclonal Antibody | Human,Mouse,Rat | WB,Elisa |
AMRe80020 | β-actin Rabbit Monoclonal Antibody | Human,Mouse,Rat | WB,ELISA |
AMM80021 | β-Tubulin Monoclonal Antibody(5G3) | Human,Rat,Mouse,Mk,Dg,Ch,Hamster,Rb,sheep,Insect,Yeast | WB,IF,IHC-p,Elisa |
EnkiLife恩玑生命相关产品
